题目内容
8.下列铁的化合物可以分别通过化合反应、置换反应、复分解反应生成的是( )| A. | FeCl2 | B. | Fe3O4 | C. | Fe(OH)3 | D. | Fe2(SO4)3 |
分析 化合反应是两种或两种以上的物质生成一种物质的反应;
置换反应是一种单质和一种化合物生成另一种单质和另一种化合物的反应;
复分解是两种化合物相互交换成分生成另外两种化合物的反应,据此分析.
解答 解:A、FeCl2可以由FeCl3和Fe的化合得到,也可以由Fe和HCl的置换得到,也可以由Fe(OH)2和HCl的复分解得到,故A正确;
B、Fe3O4能通过铁与氧气的化合反应得到,也能通过铁与水蒸气在高温条件下的置换反应得到,但无法通过复分解得到,故B错误;
C、Fe(OH)3可以通过Fe(OH)2和氧气、水的化合得到,也可以通过氯化铁与氢氧化钠的复分解得到,但无法通过置换得到,故C错误;
D、硫酸铁可以通过FeSO4溶液与氧气的化合得到,但无法通过置换得到,故D错误.
故选A.
点评 本题考查了物质的生成途径,掌握好常见的反应是解题的关键,难度不大.

练习册系列答案
相关题目
19.下表是几种弱电解质的电离平衡常数、难溶电解质的溶度积Ksp (25℃).
回答下列问题:
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为①④③②(须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式C6H5OH+PO43-=C6H5O-+HPO42-;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)=c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10mL 0.01mol/L苯酚(C6H5OH)溶液中滴加VmL 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是d;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度大于10mL 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3•H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1<T2(填>、=、<);
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是D.
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点
| 电解质 | 平衡方程式 | 平衡常数K | Ksp |
| CH3COOH | CH3COOH?CH3COO-+H+ | 1.76×10-5 | |
| H2CO3 | H2CO3?H++HCO3- HCO3-?H++CO32- | K1=4.31×10-7 K2=5.61×10-11 | |
| C6H5OH | C6H5OH?C6H5O-+H+ | 1.1×10-10 | |
| H3PO4 | H3PO4?H++H2PO4- H2PO4-?H++HPO42- HPO42-?H++PO43- | K1=7.52×10-3 K2=6.23×10-8 K3=2.20×10-13 | |
| H3BO3 | 5.7×10-10 | ||
| NH3•H2O | NH3•H2O?NH4++OH- | 1.76×10-5 | |
| H2O | Kw=1.0×10-14 | ||
| Mg(OH)2 | Mg(OH)2?Mg2++2OH- | 5.6×10-12 |
(1)由上表分析,若①CH3COOH ②HCO3- ③C6H5OH ④H2PO4-均可看作酸,则它们酸性由强到弱的顺序为①④③②(须填编号);
(2)写出C6H5OH与Na3PO4反应的离子方程式C6H5OH+PO43-=C6H5O-+HPO42-;
(3)25℃时,将等体积等浓度的醋酸和氨水混合,混合液中:c(CH3COO-)=c(NH4+);(填“>”、“=”或“<”)
(4)25℃时,向10mL 0.01mol/L苯酚(C6H5OH)溶液中滴加VmL 0.01mol/L氨水,混合溶液中粒子浓度关系正确的是d;
A.若混合液pH>7,则V≥10
B.若混合液pH<7,则c(NH4+)>c(C6H5O-)>c(H+)>c(OH-)
C.V=10时,混合液中水的电离程度大于10mL 0.01mol/L苯酚溶液中水的电离程度
D.V=5时,2c(NH3•H2O)+2c(NH4+)=c(C6H5O-)+c(C6H5OH)
(5)如图所示,有T1、T2两种温度下两条BaSO4在水中的沉淀溶解平衡曲线,回答下列问题:
①T1<T2(填>、=、<);
②讨论T1温度时BaSO4的沉淀溶解平衡曲线,下列说法不正确的是D.
A.加入Na2SO4可使溶液由a点变为b点
B.在T1曲线上方区域(不含曲线)任意一点时,均有BaSO4沉淀生成
C.蒸发溶剂可能使溶液由d点变为曲线上a、b之间的某一点(不含a、b)
D.升温可使溶液由b点变为d点

3.下列说法中,正确的是( )
| A. | 气体摩尔体积为22.4L•mol-1 | |
| B. | 1molH2的质量是2g,它所占的体积是22.4L | |
| C. | 1mol水中含有2mol氢和1mol氧 | |
| D. | 在标准状况下,1mol任何气体所占的体积都约为22.4L |
13.下列说法不正确的是( )
| A. | 甲苯和环己烯都能使酸性高锰酸钾溶液褪色 | |
| B. | 用银氨溶液可以鉴别乙醛和麦芽糖溶液 | |
| C. | 甲醛和乙二醇都可作为合成高分子化合物的单体 | |
| D. | 丙烷和2-甲基丙烷的一氯代物均为两种 |
20.己知丙烷的燃烧热△H=-2215KJ•mol-1,若一定量的丙烷完全燃烧后生成18g水,则放出的热量约为( )
| A. | 55 kJ | B. | 220 kJ | C. | 550 kJ | D. | 1108 kJ |
17.下列叙述中正确的是( )
| A. | 氯化钠溶液能导电,所以氯化钠溶液是电解质 | |
| B. | 氯化钠固体不导电,所以氯化钠不是电解质 | |
| C. | 氯化氢溶液能导电,所以氯化氢是电解质 | |
| D. | 氯气溶于水能导电,所以氯气是电解质 |
18.下列图示的化学实验操作中,正确的是( )
| A. |  倾倒液体 | B. |  取粉末状固体药品 | ||
| C. |  过滤 | D. |  浓硫酸的稀释 |
 某化学小组设计实验元素周期表中元素的性质,请回答下列问题
某化学小组设计实验元素周期表中元素的性质,请回答下列问题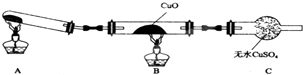 某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物NH3性质的探究.
某校研究性学习小组的同学学习完氮的有关物质的性质之后,对氮元素的氢化物NH3性质的探究.