题目内容
7.下列有关物质结构的表述正确的是( )| A. | 次氯酸的电子式 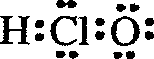 | B. | 二氧化硅分子式 SiO2 | ||
| C. | CS2结构式 S=C=S | D. | 钾离子的结构示意图如图 |
分析 A.氯原子最外层有7个电子,形成1个共价键,氧原子最外层有6个电子,形成2个共价键;
B.二氧化硅为原子晶体不存在分子,SiO2为化学式;
C.利用同族的相似性,类比二氧化碳解答;
D.原子形成离子时,核外电子数变化,质子数不变.钾离子质子数为19.
解答 解:A.氯原子最外层有7个电子,氧原子最外层有6个电子,在次氯酸中,氯原子与氧原子形成1对共用电子对,氢原子与氧原子形成1对共用电子对,都达稳定结构,电子式为 ,故A错误;
,故A错误;
B.二氧化硅为原子晶体不存在分子,晶体中有硅和氧按1:2d的比例组成,SiO2为化学式,故B错误;
C.硫元素与氧元素同族,硫原子最外层有6个电子,二硫化碳与二氧化碳的结构相似,碳原子与氧原子之间形成2对共用电子对,为直线型,其结构式为S=C=S,故C正确;
D.钾离子质子数为19,核外电子数为18,离子结构示意图 ,故D错误;
,故D错误;
故选C.
点评 本题考查了常见化学用语的书写判断,题目难度中等,涉及离子结构示意图、结构式、电子式、化学式等知识,明确离子结构示意图与原子结构示意图、化学式与分子式的区别为解答关键.

练习册系列答案
相关题目
18.甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )


| A. | 丁用于制造光导纤维 | |
| B. | 气态氢化物的稳定性:庚<己<戊 | |
| C. | 常温下,甲和乙的单质均能与水剧烈反应 | |
| D. | 丙与戊的原子序数相差28 |
2.下列反应的离子方程式书写正确的是( )
| A. | 钠与水反应:Na+H2O=Na++OH-+H2↑ | |
| B. | 铝与盐酸反应:2Al+6H+=2Al3++3H2↑ | |
| C. | 氢氧化铝与盐酸反应:OH-+H+=H2O | |
| D. | 氯化铝与氨水反应:Al3++3OH-=Al(OH)3↓ |
12.下列离子方程式中,书写正确的是( )
| A. | AlCl3溶液中加入足量的氨水:Al3++3OH-=Al(OH)3↓ | |
| B. | 往碳酸钙中滴加稀盐酸:CO32-+2H+=CO2↑+H2O | |
| C. | Na与硫酸铜溶液反应:2Na+Cu2+=Cu+2Na+ | |
| D. | 用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
17. 金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
 金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )
金属钠晶体为体心立方晶体(晶胞如图),实验测得钠的密度为ρ(g•cm-3).已知钠的相对原子质量为a,阿伏加德罗常数为NA(mol-1),假定金属钠原子为等径的刚性球且处于体对角线上的三个球相切.则钠原子的半径r(cm)为( )| A. | 3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ | B. | $\sqrt{3}$×3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ | C. | $\frac{\sqrt{3}}{4}$×3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ | D. | $\frac{1}{2}$×3$\sqrt{\frac{2a}{{N}_{Aρ}}}$ |



 .E中含氧官能团的名称为醛基和羟基.
.E中含氧官能团的名称为醛基和羟基. .写出有关反应的类型:②氧化反应⑥消去反应.
.写出有关反应的类型:②氧化反应⑥消去反应.
 或
或 (写结构简式).
(写结构简式). ;D→E
;D→E .
. 和
和 ,则鉴别G和H的试剂为溴水或溴的四氯化碳溶液.
,则鉴别G和H的试剂为溴水或溴的四氯化碳溶液. )的A的同分异构体中,其中能与NaOH溶液反应的有11种;能发生酯化反应的有
)的A的同分异构体中,其中能与NaOH溶液反应的有11种;能发生酯化反应的有 (写结构简式).
(写结构简式).