题目内容
按要求填空(1)向碳酸氢钙溶液中加入少量氢氧化钠溶液的离子方程式:______.
(2)除去FeCl3溶液中混有少量的FeCl2,应加入的试剂是______,对应化学方程式为______;除去FeCl2溶液中的少量FeCl3,应加入的试剂是______,对应离子方程式为______;除去Fe2O3中的少量Al2O3,应加入的试剂是______,对应离子方程式为______.
【答案】分析:(1)NaOH完全反应,生成碳酸钙、水、碳酸氢钠;
(2)除去FeCl3溶液中混有少量的FeCl2,可选择氯气将亚铁离子氧化,反应生成氯化铁;除去FeCl2溶液中的少量FeCl3,可选择Fe将铁离子还原为亚铁离子,反应生成氯化亚铁;除去Fe2O3中的少量Al2O3,可选择NaOH溶液将氧化铝溶解,然后过滤可得纯净的氧化铁,以此来解答.
解答:解:(1)NaOH完全反应,生成碳酸钙、水、碳酸氢钠,发生的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,
故答案为:Ca2++HCO3-+OH-=CaCO3↓+H2O;
(2)除去FeCl3溶液中混有少量的FeCl2,可选择Cl2将亚铁离子氧化,反应生成氯化铁,发生的离子反应为2Fe2++Cl2=2Fe3++2Cl-,除去FeCl2溶液中的少量FeCl3,可选择Fe将铁离子还原为亚铁离子,反应生成氯化亚铁,发生的离子反应为2Fe3++Fe=3Fe2+,除去Fe2O3中的少量Al2O3,可选择NaOH溶液将氧化铝溶解,然后过滤可得纯净的氧化铁,发生的离子反应为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Cl2;2Fe2++Cl2=2Fe3++2Cl-;Fe;2Fe3++Fe=3Fe2+;NaOH;Al2O3+2OH-=2AlO2-+H2O.
点评:本题考查离子反应方程式的书写及除杂,明确物质的性质及发生的化学反应是解答本题的关键,除杂试剂的选择是学生解答的难点,题目难度中等.
(2)除去FeCl3溶液中混有少量的FeCl2,可选择氯气将亚铁离子氧化,反应生成氯化铁;除去FeCl2溶液中的少量FeCl3,可选择Fe将铁离子还原为亚铁离子,反应生成氯化亚铁;除去Fe2O3中的少量Al2O3,可选择NaOH溶液将氧化铝溶解,然后过滤可得纯净的氧化铁,以此来解答.
解答:解:(1)NaOH完全反应,生成碳酸钙、水、碳酸氢钠,发生的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,
故答案为:Ca2++HCO3-+OH-=CaCO3↓+H2O;
(2)除去FeCl3溶液中混有少量的FeCl2,可选择Cl2将亚铁离子氧化,反应生成氯化铁,发生的离子反应为2Fe2++Cl2=2Fe3++2Cl-,除去FeCl2溶液中的少量FeCl3,可选择Fe将铁离子还原为亚铁离子,反应生成氯化亚铁,发生的离子反应为2Fe3++Fe=3Fe2+,除去Fe2O3中的少量Al2O3,可选择NaOH溶液将氧化铝溶解,然后过滤可得纯净的氧化铁,发生的离子反应为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Cl2;2Fe2++Cl2=2Fe3++2Cl-;Fe;2Fe3++Fe=3Fe2+;NaOH;Al2O3+2OH-=2AlO2-+H2O.
点评:本题考查离子反应方程式的书写及除杂,明确物质的性质及发生的化学反应是解答本题的关键,除杂试剂的选择是学生解答的难点,题目难度中等.

练习册系列答案
 计算高手系列答案
计算高手系列答案
相关题目
某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹).
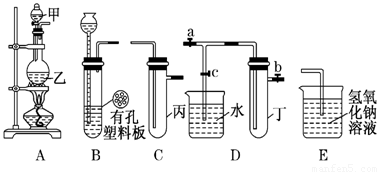
请按要求填空:
(1)仪器甲的名称是__________________;
(2)利用B装置可制取的气体有_________;(写出一种即可).
(3) A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验.
若在丙中加入适量水,即可制得氯水.将所得氯水分为两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象、结论如下:
|
实验序号 |
实验操作 |
现象 |
结论 |
|
Ⅰ |
将氯水滴入品红溶液 |
溶液褪色 |
氯气与水反应的 产物有漂白性 |
|
Ⅱ |
氯水中加入 碳酸氢钠粉末 |
有无色气泡产生 |
氯气与水反应的 产物具有酸性 |
请你评价实验Ⅰ、Ⅱ的结论是否合理?若不合理的请直接说明理由
实验Ⅰ___________________________________________________
[来源:Zxxk.Com]
实验Ⅱ____________________________________________________.
(4)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得并进行NO2有关实验.
①欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹a和b,再打开止水夹c,使烧杯中的水进入试管丁的操作是_______.
②试管丁中集满NO2,再与水充分反应后,向试管内缓缓通入一定量的氧气,直到试管内全部充满水,则所得溶液中溶质的物质的量浓度是_______mol/L(气体按标准状况计算).