题目内容
16.A、B两容器容积固定且相同,相同温度下,分别向处于真空的两容器内充气.A充入1molO2和1molNO;B中充入2moLH2S气体,下列说法正确的是( )| A. | 最终两容器中的气体压强相同 | B. | 最终两容器中的气体密度相同 | ||
| C. | A中反应时有2NA个电子转移 | D. | 最终A中气体物质的量为1.5mol |
分析 A充入的1molO2和1molNO发生反应生成1mol二氧化氮,反应后还剩余0.5mol氧气,且部分二氧化氮转化成四氧化二氮,导致气体的总物质的量小于1.5mol;B中气体的物质的量为2mol,
A.最终A、B中气体总物质的量不相等,则压强不相等;
B.密度ρ=$\frac{m}{V}$,两容器的体积相等,但气体的总质量不相等,则密度不相等;
C.1molNO完全反应生成1mol二氧化氮,转移了2mol电子;
D.根据分析可知,A中气体的总物质的量小于1.5mol.
解答 解:A充入的1molO2和1molNO发生反应生成1mol二氧化氮,反应后还剩余0.5mol氧气,且部分二氧化氮转化成四氧化二氮,导致气体的总物质的量小于1.5mol;B中气体的物质的量为2mol,
A.容器的容积固定,则压强与气体的总物质的量成正比,由于两容器中气体的物质的量不相等,则压强不相等,故A错误;
B.A充入1molO2和1molNO的总质量为:32g+28g=60g,B中1mol硫化氢的质量为34g,根据ρ=$\frac{m}{V}$可知,容器容积相等,但气体的总质量不相等,所以密度不相等,故B错误;
C.A中1molNO完全反应消耗0.5mol氧气生成1mol二氧化氮,转移了2mol电子,反应时有2NA个电子转移,故C正确;
D.由于部分二氧化氮转化成四氧化二氮,导致气体物质的量减小,则反应后气体的总物质的量小于1.5mol,故D错误;
故选C.
点评 本题考查了阿伏伽德罗定律及其推论的应用,题目难度中等,明确阿伏伽德罗定律的内容为解答关键,试题侧重考查学生的分析、理解能力及化学计算能力,D为易错点,注意部分二氧化氮转化成四氧化二氮,导致气体的总物质的量减小.

练习册系列答案
相关题目
6.某药物分子结构简式如图所示,下列关于该物质的说法不正确的是( )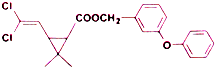

| A. | 分子式为C21H20O3Cl2 | |
| B. | 醚键上的氧原子至少与另外11个原子共面 | |
| C. | 分子中不存在手性碳原子 | |
| D. | 在一定条件下可发生加成、取代、氧化反应 |
7.胶体遇到强电解质会发生聚沉.将某溶液逐滴加入到Fe(OH)3胶体中,开始时产生沉淀,继续滴加沉淀逐渐溶解,则该溶液是( )
| A. | 1mol•L-1 NaOH溶液 | B. | 2 mol•L-1HCl溶液 | ||
| C. | 3 mol•L-1 NaCl溶液 | D. | 酒精 |
1.常温常压下,24ml氢气和氧气的混合气体,点燃反应后再恢复到原来温度和压强.剩余气体体积为3ml,则原混合气体中氢气与氧气的分子个数比可能是( )
| A. | 1:16 | B. | 16:1 | C. | 17:7 | D. | 5:7 |
8.
(1)电离平衡常数是衡量弱电解质电离程度强弱的量.上表中给出几种弱电解质的电离平衡常数,从中可以判断:在相同温度下,同浓度的三种酸溶液的导电能力由大到小的顺序为CH3COOH>H2CO3>HCN.
(2)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,三种溶液的pH由大到小的顺序为b>a>c.(填溶液前序号)
②浓度相同的NaCN溶液与CH3COOK溶液相比,c(Na+)-c(CN-)>c(K+)-c(CH3COO-).(填“>”、“<”或“=”)
③将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈酸性(填“酸”、“碱”或“中”),用离子方程式表示原因NH4++H2O?NH3•H2O+H+
④室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示.b点所示溶液中的溶质是NH3•H2O、NH4Cl
⑤NH4HCO3溶液呈碱性(填“酸”、“碱”或“中”)
(3)结合表中数据,向NaCN溶液中通入少量CO2,所发生反应的化学方程式NaCN+H2O+CO2=HCN+NaHCO3.

| 化学式 | NH3•H2O | HCN | CH3COOH | H2CO3 |
| 电离平衡常数(25℃) | Kb=1.77×10-5 | Ka=4.93×10-10 | Ka=1.76×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 |
(2)盐类水解程度的强弱同样与弱电解质的电离程度有一定联系,结合表中数据回答下列问题:
①25℃时,有等浓度的a.NaCN溶液、b.Na2CO3溶液、c.CH3COONa溶液,三种溶液的pH由大到小的顺序为b>a>c.(填溶液前序号)
②浓度相同的NaCN溶液与CH3COOK溶液相比,c(Na+)-c(CN-)>c(K+)-c(CH3COO-).(填“>”、“<”或“=”)
③将等体积等物质的量浓度的盐酸和氨水混合后,溶液呈酸性(填“酸”、“碱”或“中”),用离子方程式表示原因NH4++H2O?NH3•H2O+H+
④室温下,若将0.1mol•L-1盐酸滴入20mL 0.1mol•L-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示.b点所示溶液中的溶质是NH3•H2O、NH4Cl
⑤NH4HCO3溶液呈碱性(填“酸”、“碱”或“中”)
(3)结合表中数据,向NaCN溶液中通入少量CO2,所发生反应的化学方程式NaCN+H2O+CO2=HCN+NaHCO3.
5.在下列物质中,其物质的量为0.2mol的是( )
| A. | 0.22 g CO2 | B. | 3.6 g H2O | C. | 3.2 g O2 | D. | 73 g HCl |
 某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol•L-1)随时间(min)的变化如图所示.请回答下列问题:
某条件下,在2L密闭容器中发生如下反应:2NO2(g)?2NO(g)+O2(g),在三种不同条件下进行,其中实验Ⅰ、Ⅱ都在800℃,实验Ⅲ在850℃,NO、O2的起始浓度都为0,NO2的浓度(mol•L-1)随时间(min)的变化如图所示.请回答下列问题:
