题目内容
(1)等物质的量的CO与CO2之间:二者的质量之比为______,所含氧原子数之比为______.
(2)在标准状况下,CO和CO2混合气体的质量为32g,体积为22.4L,则其中CO所占的体积为______,CO2所占的质量为______.
解:(1)设CO与CO2的物质的量为n,则m(CO)=28ng,m(CO2)=44ng,
二者的质量之比为:m(CO):m(CO2)=28ng:44ng=7:11,
所含氧原子数之比等于氧原子物质的量之比,为:n:2n=1:2,
故答案为:7:11;1:2;
(2)设CO的物质的量为x,CO2的物质的量为y,
则
解之得:x=0.75mol,y=0.25mol,
则:V(CO)=0.75mol×22.4L/mol=16.8L,
m(CO2)=0.25mol×44g/mol=11g.
故答案为:16.8L;11g.
分析:(1)根据n= 结合分子组成计算;
结合分子组成计算;
(2)根据质量和体积列式计算可求得气体的物质的量,进而计算体积或质量.
点评:本题考查物质的量的计算,题目难度不大,注意相关计算公式的运用.
二者的质量之比为:m(CO):m(CO2)=28ng:44ng=7:11,
所含氧原子数之比等于氧原子物质的量之比,为:n:2n=1:2,
故答案为:7:11;1:2;
(2)设CO的物质的量为x,CO2的物质的量为y,
则

解之得:x=0.75mol,y=0.25mol,
则:V(CO)=0.75mol×22.4L/mol=16.8L,
m(CO2)=0.25mol×44g/mol=11g.
故答案为:16.8L;11g.
分析:(1)根据n=
 结合分子组成计算;
结合分子组成计算;(2)根据质量和体积列式计算可求得气体的物质的量,进而计算体积或质量.
点评:本题考查物质的量的计算,题目难度不大,注意相关计算公式的运用.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目
在容积为2L的密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)?2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间变化的关系分别如图1、图2所示.下列说法正确的是( )
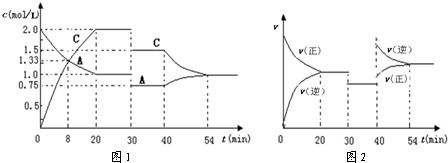

| A、0~20min用A物质表示反应的平均速率为0.05mol?L-1?min-1 | B、该反应的正反应为吸热反应 | C、x=1,且30min时改变的反应条件是减压 | D、在25min、35min、55min时化学平衡常数分别为K1、K2、K3,则K3>K2>K1 |



 ):
):
 +Cl2
+Cl2 +HCl
+HCl +3NaOH→2NaCl+H2O+
+3NaOH→2NaCl+H2O+




 )的一取代物,含有碳碳叁键.写出由X通过肽键连接而成的高聚物Y的结构简式是
)的一取代物,含有碳碳叁键.写出由X通过肽键连接而成的高聚物Y的结构简式是
 xC(g)+2D(g),经2min后达到平衡,测得D的浓度为0.4mol/L,A与B的物质的量浓度之比为1:2,C的平均反应速率是0.1mol/(L?min),求:
xC(g)+2D(g),经2min后达到平衡,测得D的浓度为0.4mol/L,A与B的物质的量浓度之比为1:2,C的平均反应速率是0.1mol/(L?min),求: