题目内容
3.现由丙二酸和乙醛等物质合成F,合成路线如下:
已知:①R1CHO+R2CH2CHO$\stackrel{一定条件}{→}$
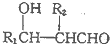 (R1、R2为烃基或H)
(R1、R2为烃基或H)②CH3OOCCH2COOCH3$→_{BrCH_{2}CH_{2}CH_{2}Cl}^{C_{2}H_{5}ONa}$
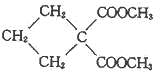 +HBr+HCl
+HBr+HCl请回答下列问题:
(1)A的官能团的名称为羟基;由逆合成分析法,推测C的结构简式
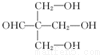 .
.(2)写出反应④的化学方程式
 .
.(3)写出符合下列条件的D的同分异构体的结构简式
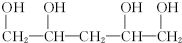 .
.①与D具有完全相同的官能团;②每个碳上最多只连接一个官能团;③核磁共振氢谱有5个吸收峰.
(4)已知F的质荷比最大值为384,在E的作用下合成F的化学反应方程式为:
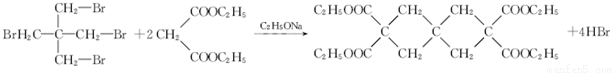 .
.
分析 乙醛与氢气发生还原反应生成乙醇,则A为CH3CH2OH,CH3CH2OH与钠反应生成E,则E为CH3CH2ONa;根据信息反应,乙醛到C的反应实质为醛和醛的加成,采用逆推法分析,碳骨架不变,则C为碳原子数为5的醛: ;C与氢气反应生成D,则D为
;C与氢气反应生成D,则D为 ;丙二酸与乙醇反应生成B,则B为:
;丙二酸与乙醇反应生成B,则B为: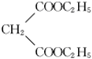 ;B与
;B与 反应生成F,根据(4)F的质荷比最大值为384,则2分子B与
反应生成F,根据(4)F的质荷比最大值为384,则2分子B与 F,反应为:
F,反应为: ,据此进行解答.
,据此进行解答.
解答 解:乙醛与氢气发生还原反应生成乙醇,则A为CH3CH2OH,CH3CH2OH与钠反应生成E,则E为CH3CH2ONa;根据信息反应,乙醛到C的反应实质为醛和醛的加成,采用逆推法分析,碳骨架不变,则C为碳原子数为5的醛: ;C与氢气反应生成D,则D为
;C与氢气反应生成D,则D为 ;丙二酸与乙醇反应生成B,则B为:
;丙二酸与乙醇反应生成B,则B为: ;B与
;B与 反应生成F,根据(4)F的质荷比最大值为384,则发生反应方程式为:
反应生成F,根据(4)F的质荷比最大值为384,则发生反应方程式为: ,
,
(1)根据分析可知,A为乙醇,含有官能团为羟基;C的结构简式为: ,故答案为:羟基;
,故答案为:羟基;  ;
;
(2)反应④为醇和卤代烃的取代反应,反应的化学方程式为: ,
,
故答案为: ;
;
(3)D为 ,其分子式为C5H12O4,①与D具有完全相同的官能团,有机物分子中含有4个醇羟基;
,其分子式为C5H12O4,①与D具有完全相同的官能团,有机物分子中含有4个醇羟基;
②每个碳上最多只连接一个官能团;③核磁共振氢谱有5个吸收峰,分子中含有5种等效H原子,说明其结构高度对称,满足以上条件的D的同分异构体的结构简式为: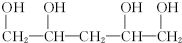 ,
,
故答案为: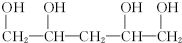 ;
;
(4)在E的作用下合成F的方程式为为: ,
,
故答案为: .
.
点评 本题考查有机合成,题目难度中等,侧重考查有机官能团的性质及相互之间的转化、有机反应方程式书写及反应类型、有条件的同分异构体的书写等相关知识,明确常见有机物结构与性质为解答关键.

练习册系列答案
相关题目
14.某元素一个原子的质量Ag,一个C-12原子的质量为Bg,NA表示阿伏加德罗常数,则该原子的摩尔质量为( )
| A. | 12A/B g•mol-1 | B. | A/NA g•mol-1 | C. | 12B/A g•mol-1 | D. | A NA g•mol-1 |
11.向某溶液中加入BaCl2溶液后观察到白色沉淀,则( )
| A. | 该溶液中一定含硫酸根离子 | |
| B. | 该溶液中一定含有银离子 | |
| C. | 该溶液中一定含有硫酸根离子和银离子 | |
| D. | 该溶液中可能含有硫酸根离子或银离子 |
18.下列推论正确的是( )
| A. | S(g)+O2(g)═SO2(g)△H1;S(s)+O2═SO2(g)△H2,则△H1>△H2 | |
| B. | C(石墨,s)═C(金刚石,s)△H=+1.9kJ•mol-1,则金刚石比石墨稳定 | |
| C. | OH-(aq)+H+(aq)=H2O(l)△H=-57.4kJ•mol-1,则:含20gNaOH的稀溶液与过量稀醋酸完全反应,放出的热量为28.7kJ | |
| D. | 2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1,则碳的燃烧热大于110.5kJ•mol-1 |
8. 如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将不会出现的现象是( )
如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将不会出现的现象是( )
 如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将不会出现的现象是( )
如图所示装置,试管中盛有水,气球a盛有干燥的固体过氧化钠颗粒,U形管中注有浅红色的水,已知过氧化钠与水反应是放热的.将气球用橡皮筋紧缚在试管口,实验时将气球中的固体颗粒抖落到试管b的水中,将不会出现的现象是( )| A. | 气球a被吹大 | B. | 试管b内有气泡冒出 | ||
| C. | U形管内红色褪去 | D. | U形管水位d高于c |
15.把384g铜粉投入含8mol硝酸和2mol硫酸的稀溶液中,则标准状况下放出的气体的物质的量为( )
| A. | 2mol | B. | 3mol | C. | 4mol | D. | 5mol |
11.甲、乙两同学在实验室分别取用不同试剂来制取Al(OH)3 可选试剂有:AlCl3溶液、A12(SO4)3溶液、NaOH溶液、氨水.
(1)请完成下表:
(2)若是你来制取Al(OH)3,试剂组合还可以是氯化铝溶液和氨水或硝酸铝溶液和氨水.
(3)由甲、乙两同学的实验现象你能得出的结论有(用简要文字说明)实验室制取氢氧化铝最好选用可溶性铝盐和氨水,氢氧化铝可以和氢氧化钠溶液发生反应,和一水合氨不发生反应.
(1)请完成下表:
| 甲同学 | 乙同学 | |
| 选用试剂 | A1C13溶液、NaOH溶液 | A12(SO4)3溶液、氨水 |
| 操作 | 向AlCl3溶液中逐滴加入NaOH溶液至过量 | 向A12(SO4)3溶液中逐滴加入氨水至过量 |
| 实验现象 | 先产生白色沉淀,然后沉淀逐渐消失 | |
| 化学方程式 | AlCl3+3NaOH=Al(OH)3↓+3NaClAl(OH)3+NaOH=NaAlO2+2H2O | A12(SO4)3+6NH3•H2O═2A1(OH)3↓+3(NH4)2SO4 |
| 离子方程式 | Al3++3OH-=Al(OH)3↓ Al(OH)3+OH-=AlO2-+2H2O | Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
(3)由甲、乙两同学的实验现象你能得出的结论有(用简要文字说明)实验室制取氢氧化铝最好选用可溶性铝盐和氨水,氢氧化铝可以和氢氧化钠溶液发生反应,和一水合氨不发生反应.
12.对室温下pH相同、体积相同的氨水和氢氧化钠溶液分别采取下列措施,其中叙述正确的是( )
| A. | 分别加水稀释10倍,两溶液的pH仍相等 | |
| B. | 温度升高10℃,两溶液的pH均不变 | |
| C. | 加入适量的氯化铵晶体后,两溶液的pH均减小 | |
| D. | 用相同浓度的盐酸中和至反应完全时,消耗盐酸的体积相同 |
