题目内容
某无色溶液中含有:①Na+、②Ba2+、③Cl-、④Br-、⑤SO32-、⑥SO42-中的一种或几种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:
根据上述实验现象,判断以下结论中正确的是( )
| 步骤 | 操作 | 现象 |
| ① | 用pH试纸检验 | 溶液的pH大于7 |
| ② | 向溶液中滴加氯水,再加入CCl4,振荡,静置 | CCl4层呈橙红色 |
| ③ | 取②的上层溶液,加入Ba(NO3)2溶液和稀HNO3 | 有白色沉淀产生 |
| ④ | 将③过滤,向滤液中加入AgNO3溶液和稀HNO3 | 有白色沉淀产生 |
A.肯定含有的离子是①④⑤
B.肯定没有的离子是②⑤
C.可能含有的离子是①②⑥
D.不能确定的离子是①③⑥
A
解析

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
下列离子方程式的书写及评价,均合理的是
| 选项 | 离子方程式 | 评价 |
| A | 将2molCl2通入到含1molFeI2的溶液中: 2Fe2++2I—+2Cl2 = 2Fe3++4Cl-+I2 | 正确;Cl2过量,可将Fe2+ 、I—均氧化 |
| B | Mg(HCO3)2溶液与足量的NaOH溶液反应: Mg2++ HCO3—+ OH—= MgCO3↓+ H2O | 正确;酸式盐与碱反应生成正盐和水 |
| C | 过量SO2通入到NaClO溶液中: SO2 + H2O + ClO- = HClO+HSO3- | 正确; 说明酸性: H2SO3强于HClO |
| D | 1mol/L的NaAlO2溶液和2.5mol/L的HCl溶液等体积互相均匀混合:2AlO2- + 5H+ = Al3+ + Al(OH)3↓+ H2O | 正确;AlO2-与Al(OH)3消耗的H+的物质的量之比为2:3 |
25℃时,下列各溶液中,离子一定能大量共存的是( )
| A.在强碱性溶液中:Na+、K+、AlO2-、Cl- |
| B.pH=1的溶液中:HCO3-、NH4+、NO3-、Ca2+ |
| C.无色溶液中:Cu2+、NO3-、Cl-、H+ |
| D.无色溶液中: Na+、K+、ClO-、SO3 2- |
下表中评价合理的是
| 选项 | 内容 | 评价 |
| A | 一定条件下0.5mol N2和1.5molH2反应,平衡时放热akJ,则N2(g)+3H2(g) 2NH3(g) 2NH3(g) 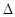 H=2akJ·mol-1 H=2akJ·mol-1 | 正确 |
| B | 氯化镁溶液与氨水反应: Mg2++2OH-=Mg(OH)2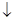 | 错误,氨水不应写成离子形式 |
| C | 向硫酸铵溶液中加入氢氧化钡溶液: Ba2++SO42-=BaSO4 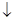 | 正确 |
| D | 等物质的量的Cl2与FeBr2在溶液中反应: 2Fe2++2Br-+2C12==2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为l:2 |
下列离子在溶液中可大量共存,形成无色透明溶液的一组是
| A.K+、Na+、OH—、MnO4- | B.Ba2+、Cu2+、NO3—、SO42— |
| C.Mg2+、Na+、OH—、SO42— | D.Cl—、Ba2+、NO3—、OH— |
下列离子方程式书写正确的是
| A.铵明矾[NH4Al(SO4)2·12H2O]溶液中加入过量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
| B.H218O中投入Na2O2固体:2H218O + 2Na2O2 = 4Na+ + 4OH- + 18O2↑ |
| C.碳酸氢钙溶液中加过量澄清石灰水:Ca2+ + OH- + HCO3- = CaCO3↓ + H2O |
D.碳酸钠的水解反应:CO32-+ H3O+ HCO3-+ H2O HCO3-+ H2O |
向含有等物质的量的NH4+、Al3+、H+的混合溶液中,慢慢滴加NaOH溶液直至过量,
并不断搅拌,依次发生了数个离子反应,则第三个离子反应是( )
| A.H++OH-=H2O |
| B.Al3++3OH-=Al(OH)3↓ |
| C.Al(OH)3+OH-=AlO2-+2H2O |
| D.NH4++OH-=NH3·H2O |
在水溶液中能大量共存的一组离子是 ( )。
| A.Na+、Ba2+、Cl-、NO3— | B.Pb2+、Hg2+、S2-、SO42— |
| C.NH4+、H+、S2O32—、PO43— | D.Ca2+、Al3+、Br-、CO32— |
下列解释实验现象的反应方程式正确的是 ( )
| A.切开的金属Na暴露在空气中,光亮表面逐渐变暗2Na+O2=Na2O2 |
| B.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgCl+S2-=Ag2S↓+2Cl- |
| C.Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物2Na2O2+2CO2=2Na2CO3+O2 |
| D.向NaHCO3溶液中加入过量的澄清石灰水,出现白色沉淀2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |