题目内容
Al溶于NaOH溶液中,有1mol Al完全反应时,做氧化剂的H2O的物质的量为( )
| A、1mol | B、3mol |
| C、4mol | D、6mol |
考点:化学方程式的有关计算
专题:
分析:Al溶于NaOH溶液发生的反应为2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑,该反应中Al作还原剂、水作氧化剂,据此分析解答.
解答:
解:Al溶于NaOH溶液发生的反应为2Al+2NaOH+6H2O=2Na[Al(OH)4]+3H2↑,该反应中Al作还原剂、水作氧化剂,根据方程式知,有1mol Al完全反应时,做氧化剂的H2O的物质的量为6mol,故选D.
点评:本题考查根据方程式的计算,正确书写方程式是解本题关键,很多同学往往认为NaOH作氧化剂而导致错误,为易错点.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
少量的金属钠长期暴露在空气中,它的最终产物是( )
| A、Na2O2 |
| B、NaHCO3 |
| C、Na2CO3 |
| D、Na2CO3?10H2O |
在一定温度下的定容密闭容器中,当下列物理量不再改变时,不能表明反应 A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A、混合气体的压强 |
| B、混合气体的密度 |
| C、混合气体的相对分子质量 |
| D、C的物质的量 |
自然界为人类提供了多种多样的营养物质,下列有关营养物质的说法正确的是( )
| A、淀粉和纤维素化学式均为(C6H10O5)n,但不互为同分异构体 |
| B、摄入人体的纤维素在酶的作用下能水解为葡萄糖 |
| C、糖类、蛋白质、油脂都属于天然高分子化合物 |
| D、所有糖类物质都有甜味,但不一定都溶于水 |
配制100mL0.1mol/L的NaCl溶液,下列操作造成配制浓度偏高的是( )
| A、定容时俯视刻度线 |
| B、没有洗涤烧杯和玻璃棒 |
| C、用托盘天平称量0.6gNaCl固体 |
| D、配制前容量瓶中残留少量的水 |
 、⑤ClCH=CHCl、⑥
、⑤ClCH=CHCl、⑥ 、⑦
、⑦ 、⑧
、⑧ 、⑨
、⑨



 单体的结构简式为
单体的结构简式为
 和
和
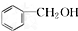 和
和
 和
和

