题目内容
 实验题:某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.
实验题:某实验小组用如图所示装置进行铜与浓硫酸反应的实验探究.(1)写出甲中反应的化学方程式:
Cu+2H2SO4
CuSO4+SO2↑+2H2O
| ||
Cu+2H2SO4
CuSO4+SO2↑+2H2O
.
| ||
(2)乙试管口的棉花应沾有的试剂是
NaOH溶液
NaOH溶液
,其作用是吸收未反应的SO2,防止污染空气
吸收未反应的SO2,防止污染空气
.(3)实验小组成员观察乙试管内液体变化是
品红溶液褪色
品红溶液褪色
.(4)充分反应后,若甲试管中有铜片剩余,继续向甲中加入NaNO3溶液,发现铜片溶解,此反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.(5)在100mL 18mol?L-1的浓硫酸中加入过量的铜片,加热使之充分反应,产生的气体在标准状况下的体积可能是
D
D
.(填字母)A.40.32L B.30.24L C.20.16L D.13.44L.
分析:(1)依据装置图分析可知铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(2)二氧化硫是污染性的气体不能排放到空气中,棉花需要沾有氢氧化钠溶液吸收二氧化硫气体;
(3)二氧化硫具有漂白性,可以使品红试液褪色;
(4)铜和稀硫酸不反应,加入的硝酸根离子,形成稀硝酸溶液氧化铜反应,铜溶解生成硝酸铜、一氧化氮和水;
(5)铜和浓硫酸反应过程中,随流水浓度减小,变为稀硫酸不能和铜继续反应,依据极值法计算分析判断;
(2)二氧化硫是污染性的气体不能排放到空气中,棉花需要沾有氢氧化钠溶液吸收二氧化硫气体;
(3)二氧化硫具有漂白性,可以使品红试液褪色;
(4)铜和稀硫酸不反应,加入的硝酸根离子,形成稀硝酸溶液氧化铜反应,铜溶解生成硝酸铜、一氧化氮和水;
(5)铜和浓硫酸反应过程中,随流水浓度减小,变为稀硫酸不能和铜继续反应,依据极值法计算分析判断;
解答:解:(1)装置图分析可知铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式为:Cu+2H2SO4
CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4
CuSO4+SO2↑+2H2O;
(2)二氧化硫是污染性的气体不能排放到空气中,棉花需要沾有氢氧化钠溶液吸收二氧化硫气体;
故答案为:NaOH溶液,吸收未反应的SO2,防止污染空气;
(3)故答案为:红溶液品褪色;
(4)中剩余的铜片继续溶解,可向其中加入硝酸钠,加入硝酸钠提供硝酸根离子和溶液中的氢离子形成稀硝酸,稀硝酸可以继续溶解铜,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(5)铜只能和浓硫酸反应,和稀硫酸不反应,Cu+2H2SO4(浓)
CuSO4+SO2↑+H2O,浓硫酸的物质的量为0.1L×18mol/L=1.8mol,如被还原的硫酸是0.9mol,则生成n(SO2)=0.9mol,V(SO2)=0.9mol×22.4L/mol=20.16L,但随着铜和浓硫酸的反应的进行,酸的浓度越来越小,不再产生二氧化硫,则生成二氧化硫的体积小于20.16L,所以选项中D符合;
故答案为:D.
| ||
故答案为:Cu+2H2SO4
| ||
(2)二氧化硫是污染性的气体不能排放到空气中,棉花需要沾有氢氧化钠溶液吸收二氧化硫气体;
故答案为:NaOH溶液,吸收未反应的SO2,防止污染空气;
(3)故答案为:红溶液品褪色;
(4)中剩余的铜片继续溶解,可向其中加入硝酸钠,加入硝酸钠提供硝酸根离子和溶液中的氢离子形成稀硝酸,稀硝酸可以继续溶解铜,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O,
故答案为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;
(5)铜只能和浓硫酸反应,和稀硫酸不反应,Cu+2H2SO4(浓)
| ||
故答案为:D.
点评:本题考查了硝酸和硫酸的性质,化学方程式的书写和判断,掌握它们的化学性质是解答的关键,题目难度中等.

练习册系列答案
相关题目
本题包括A、B两小题,分别对应于“物质结构与性质”和“实验化学”两个选修模块的内容.请选定其中一题,并在相应的答题区域内作答.若两题都做,则按A题评分.
A.《物质结构与性质》:原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36.已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
(1)X、Y、Z的电负性从大到小的顺序为______(用元素符号表示),元素Y的第一电离能大于Z的原因是______.
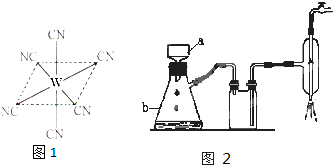
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.
①W元素基态原子价电子排布式为______.
②已知CN-与______分子互为等电子体,1molCN-中π键数目为______.
③上述沉淀溶解过程的化学方程式为______.
B.《化学实验》:无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等.某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤.除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体.
①加入少量氧化锌调节滤液使pH≈2目的是______;
②加热蒸发、浓缩溶液时,应加热到______时,停止加热.
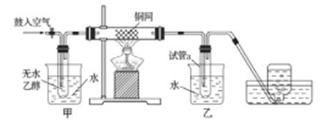
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解.停止加热,让其自然冷却、结晶.抽滤(装置如图2所示).将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体.
①写出下列仪器的名称.a______;b______.
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是______.
③用少量无水乙醇洗涤晶体的目的是______.
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量______(填“有”、“无”)影响,原因是______.
A.《物质结构与性质》:原子序数依次增大的X、Y、Z、W四种元素,原子序数均小于36.已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 496 | 4562 | 6912 | 9543 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 578 | 1817 | 2745 | 11578 |
(2)W元素应用广泛,是一种重要的生物金属元素,如人体内W元素的含量偏低,则会影响O2在体内的正常运输.已知W2+与KCN溶液反应得W(CN)2沉淀,当加入过量KCN溶液时沉淀溶解,生成配合物,其配离子结构如图所示.

①W元素基态原子价电子排布式为______.
②已知CN-与______分子互为等电子体,1molCN-中π键数目为______.
③上述沉淀溶解过程的化学方程式为______.
B.《化学实验》:无色晶体硫酸锌,俗称皓矾,在医疗上用作收敛剂,工业上作防腐剂、制造白色颜料(锌钡白)等.某实验小组欲用制氢废液制备硫酸锌晶体,进行了以下实验:
(1)取50mL制氢废液,过滤.除去不溶性杂质后,用ZnO调节滤液使pH约等于2,加热、蒸发、浓缩制得较高温度下的硫酸锌饱和溶液,冷却结晶,得到粗制的硫酸锌晶体.
①加入少量氧化锌调节滤液使pH≈2目的是______;
②加热蒸发、浓缩溶液时,应加热到______时,停止加热.
(2)粗晶体在烧杯中用适量蒸馏水溶解,滴加1~2滴稀硫酸,用沸水浴加热至晶体全部溶解.停止加热,让其自然冷却、结晶.抽滤(装置如图2所示).将所得晶体用少量无水乙醇洗涤1-2次,得到较纯的硫酸锌晶体.
①写出下列仪器的名称.a______;b______.
②抽滤跟普通过滤相比,除了得到沉淀较干燥外,还有一个优点是______.
③用少量无水乙醇洗涤晶体的目的是______.
(3)在制取氢气时,如果锌粒中混有少量的铁、铜杂质,对硫酸锌的质量______(填“有”、“无”)影响,原因是______.