��Ŀ����
A�������ֶ�����Ԫ����ɵ����Σ�X�ǻ���ɫ���壬D��F������ɫ�д̼�����ζ�����壻����I��H2������ܶ���13���ҷ����и�ԭ�Ӵ���ͬһֱ���ϣ�D��E���Ӷ���10��������ת����ϵ���£����ֲ���ʡ�ԣ���

��ش��������⣺
��1��J�Ļ�ѧʽΪ ��I�ĽṹʽΪ ��
��2����Ӧ�ݵĻ�ѧ����ʽ�ǣ� ��
��3������ת���У�����������ԭ��Ӧ���ǣ����ţ� ����Ӧ�ܵ����� ��
��4����450�桢���������£�4 mol F��2 mol O2��Ӧ����353.9 kJ����ʱ��F��ת����Ϊ90%����÷�Ӧ���Ȼ�ѧ����ʽΪ�� ��

��ش��������⣺
��1��J�Ļ�ѧʽΪ
��2����Ӧ�ݵĻ�ѧ����ʽ�ǣ�
��3������ת���У�����������ԭ��Ӧ���ǣ����ţ�
��4����450�桢���������£�4 mol F��2 mol O2��Ӧ����353.9 kJ����ʱ��F��ת����Ϊ90%����÷�Ӧ���Ȼ�ѧ����ʽΪ��
���㣺������ƶ�
ר�⣺�ƶ���
������A�������ֶ�����Ԫ����ɵ����Σ�X�ǻ���ɫ���壬��XΪCl2������I��H2������ܶ���13��˵��I��Է�������Ϊ26�������и�ԭ�Ӵ���ͬһֱ���ϣ�֤��I��CH��CH��E��10����������Y��Ӧ�õ�CH��CH��Ӧ��̼������ˮ��Ӧ����������������Ȳ��EΪH2O��YΪCaC2��HΪCa��OH��2��D����ɫ�д̼�����ζ�����壬����10����������H[Ca��OH��2]��G���ȷ�Ӧ���ɣ��ж�DΪNH3��GΪNH4Cl��F����ɫ�д̼�����ζ�����壬�����Cl2��H2O��Ӧ��˵��F��ԭ�����壬�ж�FΪSO2��AΪ��NH4��2SO3��BΪǿ�CΪ�������Σ�JΪ��������ᣬ��֤����ת����ϵ���ݴ˽��
���
�⣺A�������ֶ�����Ԫ����ɵ����Σ�X�ǻ���ɫ���壬��XΪCl2������I��H2������ܶ���13��˵��I��Է�������Ϊ26�������и�ԭ�Ӵ���ͬһֱ���ϣ�֤��I��CH��CH��E��10����������Y��Ӧ�õ�CH��CH��Ӧ��̼������ˮ��Ӧ����������������Ȳ��EΪH2O��YΪCaC2��HΪCa��OH��2��D����ɫ�д̼�����ζ�����壬����10����������H[Ca��OH��2]��G���ȷ�Ӧ���ɣ��ж�DΪNH3��GΪNH4Cl��F����ɫ�д̼�����ζ�����壬�����Cl2��H2O��Ӧ��˵��F��ԭ�����壬�ж�FΪSO2��AΪ��NH4��2SO3��BΪǿ�CΪ�������Σ�JΪ��������ᣬ��֤����ת����ϵ��
��1����������������֪JΪH2SO4��HCl��IΪ��Ȳ����ṹʽΪ��H-C��C-H��
�ʴ�Ϊ��H2SO4��HCl��H-C��C-H��
��2����Ӧ�����Ȼ�狀��������Ƽ����Ʊ������� ��Ӧ����Ӧ�Ļ�ѧ����ʽ�ǣ�2NH4Cl+Ca��OH��2
CaCl2+2NH3��+2H2O��
�ʴ�Ϊ��2NH4Cl+Ca��OH��2
CaCl2+2NH3��+2H2O��
��3��������Ӧ�Т٢ڢݢ��Ǹ��ֽⷴӦ�����Ƕ�����������������������ԭ��Ӧ�����ǰ��������������ķ�Ӧ����������ԭ��Ӧ������������ԭ��Ӧ���ǣ��ۢܣ���Ӧ�ܵķ�ӦΪ�������Ͱ�����Ӧ���ɵ������Ȼ�粒��壬����Ϊ�������������̣�
�ʴ�Ϊ���ۢܣ������������̣�
��4����450�桢���������£�4 mol SO2��2 mol O2��Ӧ����353.9 kJ����ʱ��SO2��ת����Ϊ90%����μӷ�ӦSO2Ϊ4mol��90%=3.6mol����2molSO2ȫ����Ӧ����Ϊ353.9 kJ��
=196.6KJ����÷�Ӧ���Ȼ�ѧ����ʽΪ��2SO2��g��+O2��g��=2SO3��g����H=-196.6 kJ?mol-1 ��
�ʴ�Ϊ��2SO2��g��+O2��g��=2SO3��g����H=-196.6 kJ?mol-1��
��1����������������֪JΪH2SO4��HCl��IΪ��Ȳ����ṹʽΪ��H-C��C-H��
�ʴ�Ϊ��H2SO4��HCl��H-C��C-H��
��2����Ӧ�����Ȼ�狀��������Ƽ����Ʊ������� ��Ӧ����Ӧ�Ļ�ѧ����ʽ�ǣ�2NH4Cl+Ca��OH��2
| ||
�ʴ�Ϊ��2NH4Cl+Ca��OH��2
| ||
��3��������Ӧ�Т٢ڢݢ��Ǹ��ֽⷴӦ�����Ƕ�����������������������ԭ��Ӧ�����ǰ��������������ķ�Ӧ����������ԭ��Ӧ������������ԭ��Ӧ���ǣ��ۢܣ���Ӧ�ܵķ�ӦΪ�������Ͱ�����Ӧ���ɵ������Ȼ�粒��壬����Ϊ�������������̣�
�ʴ�Ϊ���ۢܣ������������̣�
��4����450�桢���������£�4 mol SO2��2 mol O2��Ӧ����353.9 kJ����ʱ��SO2��ת����Ϊ90%����μӷ�ӦSO2Ϊ4mol��90%=3.6mol����2molSO2ȫ����Ӧ����Ϊ353.9 kJ��
| 2mol |
| 3.6mol |
�ʴ�Ϊ��2SO2��g��+O2��g��=2SO3��g����H=-196.6 kJ?mol-1��
���������⿼�������ƶϣ���Ȳ�Ʊ���Ӧ�Ͷ���������ж��ǽ���ؼ���ע��������Ŀ����ɫ����ζ��10�������Ƚ����ƶϣ���Ҫѧ���������ջ���֪ʶ���Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
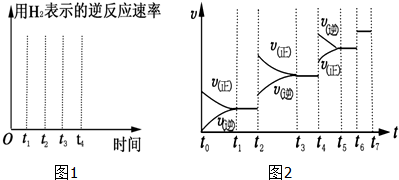
���з�Ӧ�У����ڷ�Ӧ���������Ũ�ȣ����Ըı䷴Ӧ������ǣ�������
| A����������ᷴӦ |
| B����������ۻ�ϼ��� |
| C��Al2O3��ǿ�Ӧ |
| D��������̼������������Һ��Ӧ |
 ��ѧ���ѻ���˼��������о������N4���ӣ���ṹΪ�������壨��ͼ��ʾ��������������ƣ���֪����1molN-N������193kJ����������1molN��N������941kJ��������1molN4����ת��Ϊ2molN2ʱҪ�ų�
��ѧ���ѻ���˼��������о������N4���ӣ���ṹΪ�������壨��ͼ��ʾ��������������ƣ���֪����1molN-N������193kJ����������1molN��N������941kJ��������1molN4����ת��Ϊ2molN2ʱҪ�ų�