题目内容
2013年初,雾霾天气多次肆虐天津、北京等地区.其中,燃煤和汽车尾气是造成空气污染的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)
2CO2(g)+N2(g).△H<0
①该反应平衡常数表达式 .
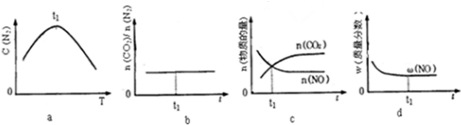
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是 (填代号).
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染.已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
2NO2(g)?N2O4(g)△H=-56.9kJ/mol
H2O(g)=H2O(l)△H=-44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式: .
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)
| 催化剂 |
①该反应平衡常数表达式
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.
煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOX可以消除氮氧化物的污染.已知:
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
2NO2(g)?N2O4(g)△H=-56.9kJ/mol
H2O(g)=H2O(l)△H=-44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:
考点:化学平衡建立的过程,用盖斯定律进行有关反应热的计算,化学平衡的影响因素
专题:基本概念与基本理论
分析:(1)①平衡常数等于生成物浓度的幂之积比上反应浓度幂之积;
②a、到达平衡后正、逆速率相等,不再变化;
b、当反应进行时,产物二氧化碳和氮气的物质的量一直按照系数比2:1在增加,所以它们的物质的量之比始终不变来判断;
c、t1时刻后二氧化碳、CO的物质的量发生变化,最后不再变化;
d、到达平衡后各组分的含量不发生变化;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式;
②a、到达平衡后正、逆速率相等,不再变化;
b、当反应进行时,产物二氧化碳和氮气的物质的量一直按照系数比2:1在增加,所以它们的物质的量之比始终不变来判断;
c、t1时刻后二氧化碳、CO的物质的量发生变化,最后不再变化;
d、到达平衡后各组分的含量不发生变化;
(2)根据盖斯定律,由已知热化学方程式乘以适当的系数进行加减构造目标热化学方程式;
解答:
解:(1)①平衡常数等于生成物浓度的幂之积比上反应浓度幂之积,即:K=
,故答案为:K=
;
②a、到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故a错误;
b、当反应进行时,产物二氧化碳和氮气的物质的量一直按照系数比2:1在增加,所以它们的物质的量之比始终不变,所以不能判断是否达到平衡,故b错误;
c、t1时刻后二氧化碳、CO的物质的量发生变化,t1时刻未到达平衡状态,故c错误;
d、NO的质量分数为定值,t1时刻处于平衡状态,故d正确,
故答案为:d;
(2)已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)?N2O4(g)△H2=-56.9kJ/mol②
H2O(g)=H2O(l)△H=-44.0kJ/mol③
根据盖斯定律,①-②+④×2可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)+2(-44.0)kJ/mol=-898.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol;
| C(N2)C 2(CO2) |
| C 2(NO)C 2(CO) |
| C(N2)C 2(CO 2) |
| C 2(NO)C2(CO) |
②a、到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故a错误;
b、当反应进行时,产物二氧化碳和氮气的物质的量一直按照系数比2:1在增加,所以它们的物质的量之比始终不变,所以不能判断是否达到平衡,故b错误;
c、t1时刻后二氧化碳、CO的物质的量发生变化,t1时刻未到达平衡状态,故c错误;
d、NO的质量分数为定值,t1时刻处于平衡状态,故d正确,
故答案为:d;
(2)已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)?N2O4(g)△H2=-56.9kJ/mol②
H2O(g)=H2O(l)△H=-44.0kJ/mol③
根据盖斯定律,①-②+④×2可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g),故△H=-867kJ/mol-(-56.9kJ/mol)+2(-44.0)kJ/mol=-898.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(g)+CO2(g)△H=-898.1kJ/mol;
点评:本题考查了盖斯定律求焓变、化学平衡影响因素,化学反应速率,平衡常数概念计算应用,注意平衡的条件分析是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列说法在一定条件下可以实现的是( )
①非金属置换金属的反应
②弱酸反应可以生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④有单质参加的非氧化还原反应.
①非金属置换金属的反应
②弱酸反应可以生成强酸
③没有水生成,也没有沉淀和气体生成的复分解反应
④有单质参加的非氧化还原反应.
| A、①②③④ | B、②④ |
| C、①②③ | D、①③④ |
可以准确判断有机化合物含有哪些官能团的分析方法是( )
| A、质谱法 |
| B、红外光谱法 |
| C、元素分析仪 |
| D、核磁共振氢谱法 |
一定量的液态化合物A在体积固定密闭容器中,在一定条件下与67.2mL X2(已转化为标准状况下)恰好完全反应A(液)+3X2(气)=B(气)+nC(气),冷却后在标准状况下,测得混合气体压强减小,则n值为( )
| A、1 | B、2 | C、3 | D、4 |
用惰性电极电解100mL CuSO4溶液一段时间后,可以通过添加0.1mol Cu(OH)2将溶液的量与浓度完全复原,则电解时电路中通过的电子为 ( )
| A、0.1mol |
| B、0.2mol |
| C、0.4mol |
| D、0.8mol 1 |
下列各组溶液不用其他试剂即能鉴别开的是( )
| A、MgCl2和NaOH |
| B、NaCl和AgNO3 |
| C、Na2CO3和HCl |
| D、AlCl3和KOH |
下列各组物质不属于同分异构体的是( )
| A、葡萄糖和果糖 |
| B、淀粉和纤维素 |
| C、蔗糖和麦芽糖 |
| D、正戊烷和新戊烷 |