题目内容
(10分)已知元素的某种性质“X”和原子半径、金属性、非金属性等一样,也是元素的一种基本性质。下面给出14种元素的X的数值:
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系___________________________;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系___________________________________。
(3)某化合物分子中含有S—N键,你认为该共用电子对偏向于_____原子(填元素符号)。
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______________。
(5)上表中元素形成的AB型化合物中,离子性最强的是________。
| 元素 | H | Li | Be | B | C | O | F |
| X的数值 | 2.20 | 0.98 | 1.57 | 2.04 | 2.55 | 3.44 | 3.98 |
| 元素 | Na | Mg | Al | Si | P | S | Cl |
| X的数值 | 0.93 | 1.31 | 1.61 | 1.90 | 2.19 | 2.58 | 3.16 |
(1)根据上表给出的数据,简述主族元素的X的数值大小与元素的金属性或非金属性强弱之间的关系___________________________;
(2)简述第二周期元素(除惰性气体外)的X的数值大小与原子半径之间的关系___________________________________。
(3)某化合物分子中含有S—N键,你认为该共用电子对偏向于_____原子(填元素符号)。
(4)经验规律告诉我们:当形成化学键的两原子相应元素的X差值大于1.7时,所形成的化学键一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中的化学键类型是______________。
(5)上表中元素形成的AB型化合物中,离子性最强的是________。
(每空2分,共10分)
(1)元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强)(2)原子半径越小,X的数值越大 (3)N (4)共价键(5)NaF
(1)元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强)(2)原子半径越小,X的数值越大 (3)N (4)共价键(5)NaF
(1)元素X的数值越大,元素的非金属性越强(或元素X的数值越小,元素的金属性越强)(2)原子半径越小,X的数值越大 (3)N原子半径小,电负性大,电子偏向N (4)Br的电负性小于Cl,3.16―1.61=1.55小于1.7,形成共价键(5)NaF,Na与F电负性差最大。
本题考查了电负性的相关知识,难度较小

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 X,试根据原子结构理论和元素周期律预测正确的是( )
X,试根据原子结构理论和元素周期律预测正确的是( ) X 位于第七周期,第ⅣB族
X 位于第七周期,第ⅣB族 和
和 的说法中不正确的是
的说法中不正确的是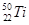 的质量数相同
的质量数相同


