题目内容
20. Mg-AgCl电池是一种用海水激活的一次电池,装置如图,其反应原理可表不为:Mg+2AgCl=MgCl2+2Ag.下列有关说法不正确的是( )
Mg-AgCl电池是一种用海水激活的一次电池,装置如图,其反应原理可表不为:Mg+2AgCl=MgCl2+2Ag.下列有关说法不正确的是( )| A. | a电极是该电池的负极 | |
| B. | b电极发生氧化反应 | |
| C. | b电极的电极反应式为:2AgCl+2e-=2Ag+2Cl- | |
| D. | 电池工作时,电子从a电极经外电路流向b电极 |
分析 该原电池中Mg易失电子作负极、AgCl是正极,负极反应式为Mg-2e-=Mg2+,正极反应式为2AgCl+2e-═2C1-+2Ag,结合转移电子相等进行计算.
解答 解:该原电池中Mg易失电子作负极、AgCl是正极,负极反应式为Mg-2e-=Mg2+,正极反应式为2AgCl+2e-═2C1-+2Ag,
A.通过以上分析知,Mg易失电子作负极,即a电极是该电池的负极,故A正确;
B.通过以上分析知,b为正极,正极发生还原反应,故B错误;
C.b为正极,正极上AgCl得电子,b电极的电极反应式为:2AgCl+2e-=2Ag+2Cl-,故C正确;
D.Mg作负极、AgCl是正极,电子从负极流向正极,则电子从a电极经外电路流向b电极,故D正确;
故选B.
点评 本题考查化学电源新型电池,题目难度不大,明确原电池原理是解本题关键,会根据失电子难易程度确定正负极,会正确书写电极反应式,为易错点.

练习册系列答案
相关题目
11.化学与生活、医疗、生产密切相关.下列物质的俗名与化学式相对应的是( )
| A. | 胆矾--FeSO4•7H2O | B. | 钡餐--BaCO3 | ||
| C. | 明矾--KAl(SO4)2 | D. | 生石膏--CaSO4•2H2O |
8.下列分散系中.分散质粒+直径最小的是( )
| A. | KC1 溶液 | B. | Fe (OH)3胶体 | C. | 牛奶 | D. | 石灰乳 |
15.下列离子可以大量共存的是( )
| A. | Fe3+、Na+、I-、Cl- | B. | Al3+、NO3-、Cl-、K+ | ||
| C. | K+、H+、HCO3-、SO42- | D. | Cu2+、Na+、SO42-、Cl- |
12.某烃和溴水反应的产物为2,2,3,3-四溴丁烷,则该烃同分异构体为( )
| A. | 1-丁烯 | B. | 1-丁炔 | C. | 2-丁炔 | D. | 2-丁烯 |
10.类比推理是化学中常用的思维方法.下列推理正确的是( )
| A. | 卤素单质的熔沸点随原子序数增大而升高,所以碱金属单质熔沸点也随原子序数增大而升高 | |
| B. | Na能与冷水反应,推测Cs也能与冷水反应 | |
| C. | Fe与Cl2反应生成FeCl3,推测Fe与S反应生成Fe2S3 | |
| D. | CO2不能与Ba(NO3)2反应,所以SO2也不能与 Ba(NO3)2反应 |


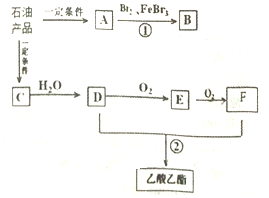 石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去).
石油是一种重要的资源,其常压蒸馏的产品在一定条件下能转化为芳香烃.A-F均为有机化合物,C的产量可以用来衡量一个国家的石油化工发展水平.它们的转化关系如图所示(部分产物和反应条件已略去). ,反应类型为取代反应;
,反应类型为取代反应;