题目内容
|
今有反应X(g)+Y(g)
| |
| [ ] | |
A. |
增大了X和Y的浓度 |
B. |
使用了催化剂 |
C. |
增加了反应体系的压强 |
D. |
升高了反应的温度 |
答案:D
解析:
解析:
精析:根据反应式,A项中X、Y的浓度增大,Z的浓度应增大,与图像不符.B项中使用催化剂,平衡不移动,浓度不再变化.C项中增大压强,X、Y和Z的浓度都增大,D项中升高温度,平衡向左移动,X、Y的浓度增大,Z的浓度减小.
小结:解答化学平衡图像题的思路是:“一读”“二想”“三判断”.
“一读”:读懂图像.读图像要学会四看:一看轴(横轴和纵轴的含意),二看点(原点、两条线的交点和线上的拐点),三看线(线的走向、线的变化趋势),四看图像中有关量的多少.
“二想”:联想规律.即联想外界条件对化学反应速率和化学平衡的影响规律.
“三判断”:作出判断.利用规律,结合图像信息,仔细分析作出正确判断.

练习册系列答案
相关题目

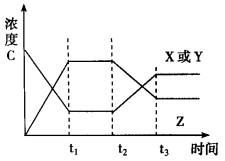

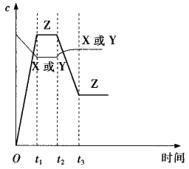
 今有反应X(g)+Y(g)
今有反应X(g)+Y(g)