题目内容
 如图是过氧化氢(H2O2)分子的空间结构示意图.
如图是过氧化氢(H2O2)分子的空间结构示意图.请回答:
(1)写出过氧化氢分子的电子式:
(2)下列关于过氧化氢的说法中正确的是
①分子中有极性键 ②分子中有非极性键 ③氧原子的轨道发生了sp2杂化 ④O-O共价键是p-p σ键 ⑤分子是非极性分子
(3)过氧化氢分子之间易形成氢键,该氢键的表示式是
(4)过氧化氢难溶于CS2,主要原因是
(5)请写出过氧化氢的两项主要用途:
考点:过氧化氢
专题:
分析:(1)根据电子式的书写方法写出过氧化氢的电子式;
(2)①H-O为极性键;
②O-O为非极性键;
③由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3;
④O的s轨道电子和O的s轨道电子成键,故是s-sσ键;
⑤过氧化氢中的键的极性不能相互抵消,是极性分子;
(3)O元素的电负性很强,O原子与H原子之间可以形成氢键;
(4)依据相似相溶的原理进行解答;H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶;
(5)过氧化氢可用做漂白剂,也可用于杀菌消毒.
(2)①H-O为极性键;
②O-O为非极性键;
③由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3;
④O的s轨道电子和O的s轨道电子成键,故是s-sσ键;
⑤过氧化氢中的键的极性不能相互抵消,是极性分子;
(3)O元素的电负性很强,O原子与H原子之间可以形成氢键;
(4)依据相似相溶的原理进行解答;H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶;
(5)过氧化氢可用做漂白剂,也可用于杀菌消毒.
解答:
解:(1)过氧化氢的电子式为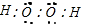 ,故答案为:
,故答案为: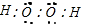 ;
;
(2)①H-O为极性键,故①正确;
②O-O为非极性键,故①正确;
③由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,故③错误;
④O的s轨道电子和O的s轨道电子成键,故是s-sσ键,故④正确;
⑤过氧化氢中的键的极性不能相互抵消,是极性分子,⑤错误;
故答案为:①②;
(3)O元素的电负性很强,O原子与H原子之间可以形成氢键,该氢键的表示式为O-H…O,故答案为:O-H…O;
(4)H2O2是极性分子,CS2是非极性分子,依据相似相溶的原理可知,H2O2难溶于CS2;H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶,故答案为:H2O2是极性分子,CS2是非极性分子;H2O2分子与H2O之间可形成氢键;
(5)过氧化氢可用做漂白剂,也可用于杀菌消毒,故答案为:做漂白剂;杀菌消毒.
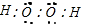 ,故答案为:
,故答案为: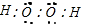 ;
;(2)①H-O为极性键,故①正确;
②O-O为非极性键,故①正确;
③由H2O2的结构可知,O原子形成1个O-H键、1个O-O键,含有2对孤对电子,杂化轨道数为4,杂化方式为sp3,故③错误;
④O的s轨道电子和O的s轨道电子成键,故是s-sσ键,故④正确;
⑤过氧化氢中的键的极性不能相互抵消,是极性分子,⑤错误;
故答案为:①②;
(3)O元素的电负性很强,O原子与H原子之间可以形成氢键,该氢键的表示式为O-H…O,故答案为:O-H…O;
(4)H2O2是极性分子,CS2是非极性分子,依据相似相溶的原理可知,H2O2难溶于CS2;H2O2中氧元素的电负性很强,H2O2分子H2O分子之间形成氢键,使H2O2与水任意比互溶,故答案为:H2O2是极性分子,CS2是非极性分子;H2O2分子与H2O之间可形成氢键;
(5)过氧化氢可用做漂白剂,也可用于杀菌消毒,故答案为:做漂白剂;杀菌消毒.
点评:本题考查的知识点较多,难度较大,涉及电子式的书写、氢键的表示方法、化学键的形成方式及键的极性和分子的极性判断、相似相溶的原理的应用、物质的用途等,要注意基础知识的积累.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
能够确定一种溶液中一定含有SO42-的事实是( )
| A、取少量试样溶液,加入用硝酸酸化过的BaCl2中,有白色沉淀生成 |
| B、取少量试样溶液,加入BaCl2溶液,有白色沉淀,再加稀HNO3有白色沉淀生成 |
| C、取少量试样溶液加入Ba(NO3)2溶液,有白色沉淀 |
| D、取少量试样溶液加入足量的盐酸无沉淀,加入BaCl2,有白色沉淀生成 |
下列气体中,能污染空气又不易被察觉的是( )
| A、O2 |
| B、H2S |
| C、CO |
| D、NO |
可证明次氯酸是弱酸的实验事实是( )
| A、可与碱发生中和反应 |
| B、次氯酸有漂白性 |
| C、次氯酸见光分解 |
| D、次氯酸钙溶液中通入CO2,生成次氯酸 |
下列基本实验操作中,正确的是( )
A、 |
B、 |
C、 |
D、 |
下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL 水 ④0.2mol H3PO4.
①0.5mol NH3 ②标准状况下22.4L He ③4℃9mL 水 ④0.2mol H3PO4.
| A、①④③② | B、④③②① |
| C、②③④① | D、①④③② |

 如图是研究甲烷取代反应实验装置图,具体的实验方法是:取一个100mL的大量筒,用排饱和食盐水的方法先后收集20mLCH4和80mLCl2,进行实验.
如图是研究甲烷取代反应实验装置图,具体的实验方法是:取一个100mL的大量筒,用排饱和食盐水的方法先后收集20mLCH4和80mLCl2,进行实验.