题目内容
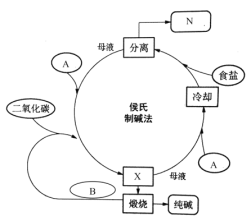
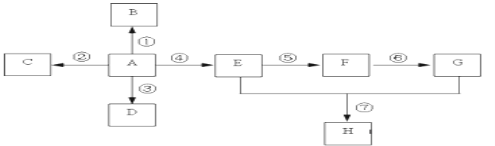
【题目】A~F各物质间转化关系如下图所示。A为常见气态烃,其产量可作为一个国家石油化工发展水平的标志,B和D是生活中常见有机物,D能跟Na2CO3溶液反应,F有香味。
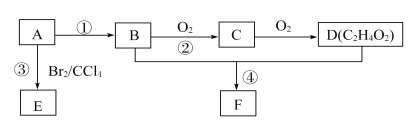
(1)E的结构简式为____________,实验室中②的反应条件是____________。
(2)A可合成高分子化合物PE,PE可用于制备保鲜膜、食品袋等,A合成PE的化学反应方程式为____________,该反应类型是____________。
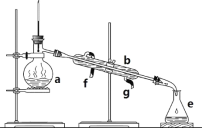
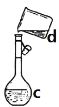
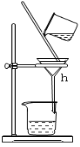
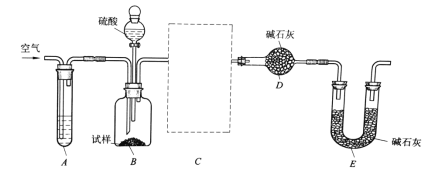
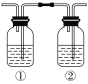
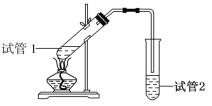
(3)实验室制备F时装置如图,试管2中所盛液体是饱和Na2CO3溶液。试管1中反应结束后,试管2中液体量比反应前增多且分层。振荡试管2后发现上层有机层液体变少,则振荡时发生的化学反应方程式为____________。
【答案】CH2BrCH2Br Cu催化、加热 nCH2=CH2![]()
![]() 加聚反应 Na2CO3+2CH3COOH=2CH3COONa+CO2↑+H2O或Na2CO3+CH3COOH=CH3COONa+NaHCO3
加聚反应 Na2CO3+2CH3COOH=2CH3COONa+CO2↑+H2O或Na2CO3+CH3COOH=CH3COONa+NaHCO3
【解析】
A为常见气态烃,其产量可作为一个国家石油化工发展水平的标志,是乙烯,反应③是乙烯和溴的四氯化碳溶液发生加成反应,生成E为1,2-二溴乙烷,结构简式为:CH2BrCH2Br,B和D是生活中常见有机物,D能跟Na2CO3溶液反应,是乙酸,F有香味,是乙酸乙酯,B是乙醇,由乙烯和水发生加成反应制得,B和氧气反应生成乙醛,C是乙醛,乙醛和氧气反应生成乙酸,乙酸和乙醇发生酯化反应得到F为乙酸乙酯,据此分析。
(1) 反应③是乙烯和溴的四氯化碳溶液发生加成反应,生成E为1,2-二溴乙烷,E的结构简式为CH2BrCH2Br,②是乙醇催化氧化成乙醛的反应,催化氧化的反应条件Cu催化、加热;
(2)A可合成高分子化合物PE,PE可用于制备保鲜膜、食品袋等,PE是聚乙烯,乙烯合成聚乙烯的化学反应方程式为:nCH2=CH2![]()
![]() ,该反应类型是加聚反应;
,该反应类型是加聚反应;
(3)乙酸和乙醇制取乙酸乙酯后,试管2上方有有机层乙酸乙酯和挥发出的乙酸和乙醇,振荡试管2后发现上层有机层液体变少,是乙酸与碳酸钠发生反应,化学方程式为:Na2CO3+2CH3COOH=2CH3COONa+CO2↑+H2O或Na2CO3+CH3COOH=CH3COONa+NaHCO3。

 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案