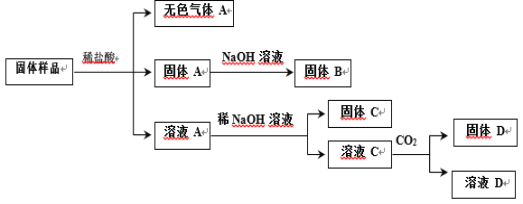
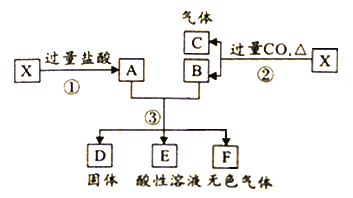
题目内容
【题目】二甲醚和乙醇是两种常见的有机溶剂,也可作为新能源。
(1)通过以下反应可获得二甲醚(CH3OCH3):
①CO(g)+H2O(g)=CO2(g)+H2(g) ΔH 1=a kJ·molˉ1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH 2=b kJ·molˉ1
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH 3=c kJ·molˉ1
则反应 2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的 ΔH=_________kJ·molˉ1。
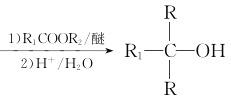
(2)已知气相直接水合法可以制取乙醇:H2O(g)+C2H4(g) ![]() CH3CH2OH(g)。
CH3CH2OH(g)。
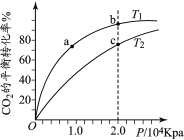
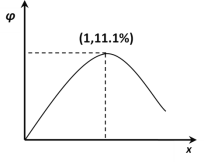
在 n(H2O)∶n(C2H4)=1∶1 的条件下投料,乙烯的平衡转化率与温度(T)及压强(p) 的关系如图1所示。
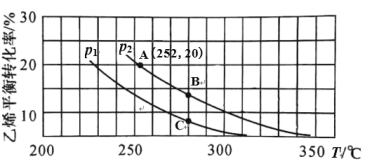 图1
图1
①下列有关说法中正确的是_________。
A.p1>p2 B.280℃时,vB>vC
C.A、B、C 三点的平衡常数 KA>KB>KC D.低温有利于该反应自发进行
②在 p2,280℃条件下,C 点的 v 正 ____v 逆 (填“>”、“<”或“=”),理由是________。
③计算图 1 中 A 点的平衡常数 Kp=_________。(结果用 p2 的代数式表示,平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
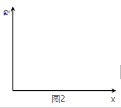
(3)在 n(H2O)∶n(C2H4)=1∶x 的条件下投料,某研究小组在压强为 p2,温度为 252℃ 时,进行平衡体系中乙醇的体积分数随投料比变化的测定实验。在图 2 中画出平衡体系中乙醇的体积分数 φ 随 x 变化的示意图____。
【答案】2a+2b+c BD > 在p2,280℃条件下,平衡转化率在B点位置,说明C点未达平衡状态,反应正向进行 ![]()
【解析】
(1)通过以下反应可获得二甲醚(CH3OCH3):
①CO(g)+H2O(g)=CO2(g)+H2(g) ΔH 1=a kJ·molˉ1
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH 2=b kJ·molˉ1
③2CH3OH(g)=CH3OCH3(g)+H2O(g) ΔH 3=c kJ·molˉ1
由盖斯定律,2×①+2×②+③得:反应 2CO(g)+4H2(g)=CH3OCH3(g)+H2O(g)的 ΔH=(2a+2b+c)kJ·molˉ1。
故答案为:2a+2b+c;
(2)①A.当温度相同时,从p1到p2乙烯转化率增大,平衡正向移动,p1<p2 ,故A错误;
B.280℃时,B点压强大,vB>vC,故B正确;
C.压强为P2时升高温度,乙烯转化率减小,平衡常数减小,但BC温度相同,平衡常数相同,A、B、C 三点的平衡常数 KA>KB=KC ,故C错误;
D.升高温度,乙烯转化率减小,△H<0,△S<0,低温有利于该反应自发进行,故D正确;
故答案为:BD;
②在 p2,280℃条件下,C 点的 v 正>v 逆;理由是:在p2,280℃条件下,平衡转化率在B点位置,说明C点未达平衡状态,反应正向进行;
故答案为:>;在p2,280℃条件下,平衡转化率在B点位置,说明C点未达平衡状态,反应正向进行;
③计算图 1 中 A 点的平衡常数:
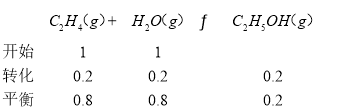
乙醇占![]() =
=![]() ,乙烯和水各占
,乙烯和水各占![]() =
=![]() ,Kp=
,Kp=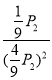
![]() 。故答案为:
。故答案为:![]() ;
;
(3)在 n(H2O)∶n(C2H4)=1∶x 的条件下投料,某研究小组在压强为 p2,温度为 252℃ 时,进行平衡体系中乙醇的体积分数随投料比变化的测定实验。n(H2O)∶n(C2H4)=1∶1时,乙烯的转化率最大,![]() ,或11.1%,画出平衡体系中乙醇的体积分数 φ 随 x 变化的示意图
,或11.1%,画出平衡体系中乙醇的体积分数 φ 随 x 变化的示意图![]() 。
。
故答案为: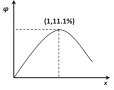 ;
;

 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案【题目】I.(1) SiH4是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2(s)和H2O(l)。已知室温下2 g SiH4自燃放出的热量为89.2 kJ,则其热化学方程式为: _____________________。
(2)沼气是一种能源,它的主要成分是CH4,其燃烧的热化学方程式为:CH4(g)+2O2(g) = CO2(g)+2H2O(l ) ΔH=-890 kJ/mol,又已知H2O(l)=H2O(g) ΔH=+44 kJ/mol,则11.2 L(标准状况)CH4完全燃烧生成气态水时放出的热量为_______________。
Ⅱ.已知下列几种烷烃的燃烧热如下:
烷烃 | 甲烷 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
燃烧热/ (kJ·mol-1) | 890.3 | 1559.8 | 2219.9 | 2877.0 | 3536.2 | 4163.1 |
今有10 L(标准状况下)某种天然气,假设仅含甲烷和乙烷两种气体,燃烧时共放出热量480 kJ。
(1)试写出乙烷气体燃烧的热化学方程式___________________________________。
(2)计算该天然气中甲烷的体积分数____________(保留小数点后两位)。
(3)由上表可总结出的近似规律是______________________________________________。
(4)根据(3)的近似规律可预测癸烷的燃烧热约为______kJ·mol-1。