题目内容
氯气是一种重要的化工原料,在生产和生活中应用十分广泛.已知:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O,所以在实验室可用高锰酸钾固体和浓盐酸制氯气.
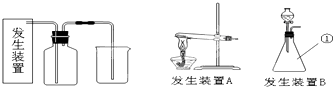
(1)仪器①的名称
(2)在上述反应中,氧化剂是
(3)当集气瓶中收集满氯气时,可以观察到气体呈
(4)工业上电解饱和食盐水制取氯气的化学方程式:
分析:(1)依据装置图中仪器形状和作用分析名称;在实验室可用高锰酸钾固体和浓盐酸制氯气不需要加热,发生装置选择B;
(2)反应中元素化合价降低的物质做氧化剂;
(3)氯气是黄绿色气体;
(4)电解饱和食盐水阳极上氯离子失电子生成氯气,阴极上氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大形成氢氧化钠;
(2)反应中元素化合价降低的物质做氧化剂;
(3)氯气是黄绿色气体;
(4)电解饱和食盐水阳极上氯离子失电子生成氯气,阴极上氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大形成氢氧化钠;
解答:解:(1)装置B中②是锥形瓶;实验室可用高锰酸钾固体和浓盐酸制氯气不需要加热,制备氯气的发生装置选择B;
故答案为:锥形瓶;B;
(2)在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中,锰元素化合价从+7价变化为+2价,元素化合价降低,高锰酸钾做氧化剂;
故答案为:KMnO4;
(3)氯气是黄绿色气体,当集气瓶中收集满氯气时,可以观察到气体呈黄绿色;
故答案为:黄绿色;
(4)电解饱和食盐水阳极上氯离子失电子生成氯气,阴极上氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大形成氢氧化钠,反应的化学方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑;
故答案为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑.
故答案为:锥形瓶;B;
(2)在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中,锰元素化合价从+7价变化为+2价,元素化合价降低,高锰酸钾做氧化剂;
故答案为:KMnO4;
(3)氯气是黄绿色气体,当集气瓶中收集满氯气时,可以观察到气体呈黄绿色;
故答案为:黄绿色;
(4)电解饱和食盐水阳极上氯离子失电子生成氯气,阴极上氢离子得到电子生成氢气,溶液中氢氧根离子浓度增大形成氢氧化钠,反应的化学方程式为:2NaCl+2H2O
| ||
故答案为:2NaCl+2H2O
| ||
点评:本题考查了实验室制备氯气的方法和原理分析,氯气性质的分析应用,掌握基础是关键,题目较简单.

练习册系列答案
相关题目