题目内容
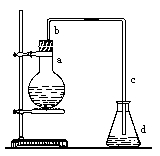
实验室用下图装置制取乙酸乙酯。

(1)在大试管中配制一定比例的乙醇、乙酸和浓H2SO4的混合液的方法是 。
(2)加热前,大试管中加入几粒碎瓷片的作用是 ,导气管不能插入饱和Na2CO3溶液中是为了 。
(3)浓H2SO4的作用是 。
(4)饱和Na2CO3溶液的作用是_________________________。
(5)实验室生成的乙酸乙酯,其密度比水________(填“大”或“小”),有______气味。
⑹有甲、乙、丙三位同学,分别将乙酸与乙醇反应得到的酯(未用饱和Na2CO3溶液承接)提纯,在未用指示剂的情况下,他们都是先加NaOH中和过量的酸,然后用蒸馏法将酯分离出来。但他们的结果却不同:
①甲得到了不溶于水的中性酯;
②乙得到显酸性的酯的混合物;
③丙得到大量水溶性物质。
试分析产生上述各种现象的原因。
⑺下图是某同学探究“分离乙醇乙酯、乙醇、乙酸混合物”实验操作步骤流程图。
请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法,在方框内填入所分离的有关物质的名称。
 |
【解析】本道题即注重了对基础知识的考察,又拓展了学生的探究能力,对实验中学生可能出现的问题进行考察,从而可使学生重视平时的探究实验,督促自己多动手做实验;并注意积累实验经验,分析原因,从而提高分析问题、解决问题的能力
【答案】
(1)将浓H2SO4慢慢加入乙醇和乙酸的混合液中
(2)防止暴沸 防止倒吸
(3)①催化剂 ②吸水剂,有利于平衡向酯化反应方向移动
(4)除去酯中混有的乙酸和乙醇,降低酯在水中溶解度,易于分层
(5)小 果香味
⑹①甲同学加入的碱正好将过量的酸中和,所以蒸馏后得到中性酯;②乙同学加入碱量不足,所以蒸馏出来的有过量的酸,得到显酸性的酯的混合物;③丙同学加入的碱过量使生成的酯已经水解为可溶性的醇和钠盐。
⑺

 名师点拨卷系列答案
名师点拨卷系列答案