题目内容
18. 香豆素-4是一种激光染料,应用于可调谐染料激光器.香豆素-4由C、H、O三种元素组成,分子球棍模型如图所示.下列有关叙述正确的是( )
香豆素-4是一种激光染料,应用于可调谐染料激光器.香豆素-4由C、H、O三种元素组成,分子球棍模型如图所示.下列有关叙述正确的是( )①分子式为C10H9O3
②能与饱和溴水发生取代反应
③能与饱和溴水发生加成反应
④能使酸性KMnO4溶液褪色
⑤1mol香豆素-4最多能与含1molNaOH的溶液反应.
| A. | ①②③ | B. | ③④⑤ | C. | ②③④ | D. | ②③④⑤ |
分析 根据有机物的价键规则(碳原子形成4条键,氧原子形成2条键,氢原子形成1条键)可写出该有机物的结构简式为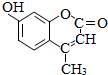 ,含酚-OH、C=C、-COOC-,结合苯酚、烯烃、酯的性质来解答.
,含酚-OH、C=C、-COOC-,结合苯酚、烯烃、酯的性质来解答.
解答 解:①分子式为C10H8O3,故错误;
②含有碳碳双键,所以能与Br2水发生加成反应,含有酚羟基且苯环上酚羟基的邻位有氢原子,所以能与溴水发生取代反应,故正确;
③香豆素-4中含有碳碳双键,能与溴水发生加成反应,故正确;
④含有碳碳双键,所以能使酸性KMnO4溶液褪色,故正确;
⑤含有酚羟基和酯基,且酯基可水解生成酚羟基,则1mol香豆素-4最多能与含3molNaOH的溶液反应,故错误;
故选C.
点评 本题考查有机物的结构与性质,为高考常见题型,把握官能团及性质的关系为解答的关键,熟悉苯酚、烯烃的性质为即可解答,题目难度不大.

练习册系列答案
相关题目
3.下列实验方案正确且能达到预期目的是( )
| 选项 | 实验方案 | 实验目的或结论 |
| A | 将H2SO4酸化的H2O2滴入Fe(NO3)2溶液中,溶液变黄色 | 氧化性:H2O2比Fe3+强 |
| B | 将SO2通入酸性高锰酸钾溶液中 | SO2具有漂白性 |
| C | 取a g铝箔与足量氢氧化钠溶液充分反应,逸出的气体通过浓硫酸后,测其体积为V L(标况) | 测定铝箔中氧化铝的含量 |
| D | 比较不同反应的反应热数据大小 | 判断反应速率大小 |
| A. | A | B. | B | C. | C | D. | D |
6.下列说法正确的是( )
| A. |  与丙三醇互为同系物 与丙三醇互为同系物 | |
| B. |  与 与 的单体相同 的单体相同 | |
| C. | 淀粉、蛋白质、光导纤维均为有机高分子化合物 | |
| D. | 按系统命名法,化合物 的名称为 2-甲基-3,4-乙基己烷 的名称为 2-甲基-3,4-乙基己烷 |
13.已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱.下列反应在水溶液中不可能发生的是( )
| A. | 3 Cl2+6 FeI2=2FeCl3+4 FeI3 | B. | 3Cl2+2FeI2=2FeCl3+2I2 | ||
| C. | Co2O3+6 HCl=2CoCl2+Cl2↑+3H2O | D. | 2FeCl3+2HI=2FeCl2+I2+2HCl |
3.下列说法不正确的是( )
| A. | 硬脂酸甘油酯在碱性条件下的水解是皂化反应 | |
| B. | 所有糖类、油脂、蛋白质都能发生水解反应 | |
| C. | 往蛋白质溶液中加入饱和硫酸铵溶液,产生的沉淀再加水又可溶解 | |
| D. | 氨基酸能够以不同数目和顺序相结合形成结构复杂的多肽 |
10.下列反应中气体作氧化剂的是( )
| A. | SO2通入水中:SO2+H2O=H2SO3 | |
| B. | Cl2通入FeCl2溶液中:Cl2+2FeCl2=2FeCl3 | |
| C. | HCl通入NaOH溶液中:HCl+NaOH=NaCl+H2O | |
| D. | CO2通入NaOH溶液中:CO2+2NaOH=Na2CO3+H2O |
5.某元素二价阴离子的核外有10个电子,质量数为18,该元素的原子核中的中子数为( )
| A. | 10 | B. | 8 | C. | 18 | D. | 28 |




