题目内容
(8分)(1)写出离子方程式:
硫酸钠溶液与氯化钡溶液
铝片与硝酸汞溶液 。
(2)写出与下列离子方程式相对应的化学方程式:
H+ + OH-= H2O
Cu2+ + Fe= Cu + Fe2+ 。
【答案】
(1)Ba2++SO42-=BaSO4↓ 2Al+3Hg2+=2Al3++3Hg
(2)HCl+NaOH=NaCl+H2O CuSO4+Fe=FeSO4+Cu
【解析】考查常见化学用语的书写。在离子方程式中要把同时满足易溶和易电离的物质用离子符号表示,其余物质全部用化学式表示。

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
(12分)为研究温度对Cl2与KOH反应的影响,设计实验如下:
在蒸馏烧瓶中装入足量MnO2,分液漏斗中装足量浓盐酸,大试管A中装4mol/LKOH溶液15mL,并置于75℃水浴中,大试管B中装02mol/LKOH溶液,并置于冰水中,C中装NaOH溶液。
试回答下列问题:
(1)水浴加热有什么优点?
(2)如何判断A中已经反应完全?
(3)分离A中生成的两种盐,检测发现其中KCl为005mol(不考虑HCl挥发),写出A中发生的化学方程式
(4)分离B中生成的两种盐, 其物质的量之比为1:1,写出离子方程式。
其物质的量之比为1:1,写出离子方程式。
(5)试管B要置于冰水中降温的主要原因是:
| A.从试管A中出来的气体温度较高,易使试管B中的溶液温度升高 | |
| B.防止生成的盐分解 | C.催化剂在冷水中活性最强 |
| D.该反应是放热反应,为防止温度过高,采用降温 |
 可以用图二代替吗?。
可以用图二代替吗?。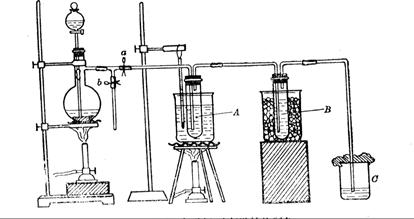
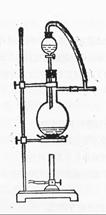
图一 图二