题目内容
等体积、pH相同的氨水与NaOH溶液,下列说法正确的是( )
| A、分别加水稀释相同的倍数,稀释后两溶液pH仍相同 | B、NaOH溶液中水电离产生的c(OH-)较小 | C、用等浓度的盐酸完全中和,消耗盐酸体积相等 | D、加入少量NH4Cl(s),pH均减小 |
分析:A、一水合氨为弱电解质,溶液中部分电离,稀释后氨水中氢氧根离子的物质的量增大,氢氧化钠溶液中氢氧根离子的物质的量不变;
B、碱溶液中氢离子为水电离的,溶液的pH相同,水电离的氢离子和氢氧根离子浓度相同;
C、氨水为弱碱,氨水的浓度大于氢氧化钠溶液的浓度,所以氨水消耗的等浓度的盐酸的体积大与氢氧化钠溶液;
D、两溶液中加入氯化铵,溶液中氢氧根离子浓度减小,溶液的pH减小.
B、碱溶液中氢离子为水电离的,溶液的pH相同,水电离的氢离子和氢氧根离子浓度相同;
C、氨水为弱碱,氨水的浓度大于氢氧化钠溶液的浓度,所以氨水消耗的等浓度的盐酸的体积大与氢氧化钠溶液;
D、两溶液中加入氯化铵,溶液中氢氧根离子浓度减小,溶液的pH减小.
解答:解:A、一水合氨为弱电解质,溶液中部分电离出氢氧根离子,稀释后一水合氨的电离程度增大,溶液中氢氧根离子的物质的量增大,所以稀释相同的倍数后,氨水的pH大于氢氧化钠溶液的,故A错误;
B、氨水和氢氧化钠溶液都为碱溶液,溶液中氢离子为水电离的,溶液的pH相同,所以两溶液中水电离程度相同,水电离的氢氧根离子浓度相同,故B错误;
C、由于一水合氨为弱电解质,pH相同时氨水浓度大于氢氧化钠溶液的浓度,所以用等浓度的盐酸完全中和,氨水消耗盐酸体积大于氢氧化钠溶液消耗盐酸体积,故C错误;
D、氨水中加入氯化铵,铵离子浓度增大,抑制了氨水的电离,溶液中氢氧根离子浓度减小,溶液pH减小;氢氧化钠溶液中加入氯化铵,铵离子与氢氧根离子反应生成弱电解质一水合氨,导致溶液中氢氧根离子浓度减小,溶液的pH减小,故D正确;
故选D.
B、氨水和氢氧化钠溶液都为碱溶液,溶液中氢离子为水电离的,溶液的pH相同,所以两溶液中水电离程度相同,水电离的氢氧根离子浓度相同,故B错误;
C、由于一水合氨为弱电解质,pH相同时氨水浓度大于氢氧化钠溶液的浓度,所以用等浓度的盐酸完全中和,氨水消耗盐酸体积大于氢氧化钠溶液消耗盐酸体积,故C错误;
D、氨水中加入氯化铵,铵离子浓度增大,抑制了氨水的电离,溶液中氢氧根离子浓度减小,溶液pH减小;氢氧化钠溶液中加入氯化铵,铵离子与氢氧根离子反应生成弱电解质一水合氨,导致溶液中氢氧根离子浓度减小,溶液的pH减小,故D正确;
故选D.
点评:本题考查了弱电解质的电离、溶液pH的简单计算,题目难度中等,注意明确弱电解质的电离情况,掌握溶液酸碱性与溶液pH的关系.

练习册系列答案
相关题目
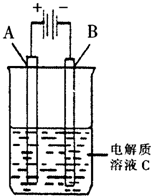 (2011?丹东模拟)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料.
(2011?丹东模拟)肼(N2H4)又称联氨,是一种可燃性液体,其燃烧热较大且燃烧产物对环境无污染,故可以用作火箭燃料. N2H+5+OH-;N2H+5+H2O
N2H+5+OH-;N2H+5+H2O