题目内容
【题目】右图为以惰性电极进行电解:
(1)写出A、B、C、D各电极上的电极反应式和总反应方程式:
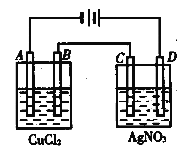
A:________________,B:__________________,总反应方程式:________________________;C:________________________________,D:________________________________,总反应方程式:___________________________;
(2)在A、B、C、D各电极上析出生成物的物质的量比为__________________。
【答案】 Cu 2+ +2e - = Cu 2Cl - -2e-=Cl 2 ↑ CuCl 2![]() Cu+ Cl 2 ↑ 4Ag + +4e - =4Ag 4OH - -4e - =2H 2 O+O 2 ↑ 4AgNO 3 +2H 2 O
Cu+ Cl 2 ↑ 4Ag + +4e - =4Ag 4OH - -4e - =2H 2 O+O 2 ↑ 4AgNO 3 +2H 2 O![]() Ag+O 2 ↑+4HNO 3 2:2:4:1
Ag+O 2 ↑+4HNO 3 2:2:4:1
【解析】(1)A极连接电源的负极,A是阴极,溶液中的铜离子放电,电极反应式是Cu2++2e-= Cu,B是阳极,溶液中的氯离子放电,电极反应式是2Cl--2e-=Cl2↑;所以总反应方程式是CuCl2![]() Cu+ Cl2↑;D电极和电源的正极相连,所以D电极是阳极,溶液中的OH-放电,电极反应式是4OH--4e-=H2O+O2↑;C是阴极,溶液中的银离子放电,电极反应式是4Ag++4e-=4Ag,总反应方程式是4AgNO3+2H2O
Cu+ Cl2↑;D电极和电源的正极相连,所以D电极是阳极,溶液中的OH-放电,电极反应式是4OH--4e-=H2O+O2↑;C是阴极,溶液中的银离子放电,电极反应式是4Ag++4e-=4Ag,总反应方程式是4AgNO3+2H2O![]() Ag+O2↑+4HNO3; (2)根据电子的得失守恒(可以根据上述电极反应式中各物质分别得失电子数相等时的电极产物计算)可知,在A、B、C、D各电极上析出生成物的物质的量比为2︰2︰4︰1。
Ag+O2↑+4HNO3; (2)根据电子的得失守恒(可以根据上述电极反应式中各物质分别得失电子数相等时的电极产物计算)可知,在A、B、C、D各电极上析出生成物的物质的量比为2︰2︰4︰1。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目