题目内容
【题目】回答下列问题
(1)8.4g N2与9.6g某单质Rx所含原子个数相同,且分子数之比为3:2,则R的相对原子质量是 , x值为 .
(2)4.5g水与g硫酸所含的分子数相等,它们所含氧原子数之比是 , 其中氢原子数之比是 .
(3)如图所示,分别向密闭容器内可移动活塞的两边充入空气(已知空气体积占整个容器容积的1/4)、H2和O2的混合气体,在标准状况下,若将H2、O2的混合气体点燃引爆.活塞先左弹,恢复原温度后,活塞右滑停留于容器的中央.则原来H2、O2的体积之比可能为 . 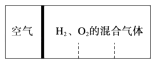
【答案】
(1)16;3
(2)24.5;1:4;1:1
(3)7:2 或4:5
【解析】解:(1.)n(N2)= ![]() =0.3mol,N原子的物质的量为0.6mol,8.4gN2与9.6g某单质R所含的原子个数相同,则9.6g某单质Rx中所含原子个数为0.6NA , 分子数之比为3:2,所以N2与RX相对分子质量之比
=0.3mol,N原子的物质的量为0.6mol,8.4gN2与9.6g某单质R所含的原子个数相同,则9.6g某单质Rx中所含原子个数为0.6NA , 分子数之比为3:2,所以N2与RX相对分子质量之比 ![]() :
: ![]() =7:12,
=7:12,
而N2相对分子质量为28,所以Rx相对分子质量=28× ![]() =48,
=48,
又因为两者所含原子个数相同,即3×2=2x,
得x=3,
所以R的相对原子质量= ![]() =16,
=16,
所以答案是:16;3;
(2.)水与硫酸分子数相等,则二者物质的量相等: ![]() =
= ![]() =0.25mol,解得m(H2SO4)=24.5g;
=0.25mol,解得m(H2SO4)=24.5g;
含有氧原子数之比为:0.25mol×1:0.25mol×4=1:4;含有氢原子数之比为:0.25mol×2:0.25mol×2=1:1;
所以答案是:24.5;1:4;1:1;
(3.)令空气的物质的量为1mol,反应前,左右两室的体积之比为1:3,反应前右室的物质的量为3mol,反应后,活塞处于中央,两室体积相等,则两室中气体的物质的量相等,反应后右室气体物质的量为1mol,发生反应2H2+O2 ![]() 2H2O,
2H2O,
设H2、O2的物质的量分别为xmol、ymol,
若氢气过量,则:x﹣2y=1,x+y=3,解得x:y=7:2,
若氧气过量,则:y﹣0.5x=1,x+y=3,解得x:y=4:5,
所以答案是:7:2 或4:5.

 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案