题目内容
将0.1mol/L的NH3?H2O溶液加水稀释,下列说法正确的是( )
A、
| ||
| B、OH-个数将减少 | ||
C、
| ||
| D、NH4+浓度将减小 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:加水稀释促进NH3?H2O电离,溶液中c(NH4+)、c(OH-)、c(NH3.H2O) 都减小,c(H+)增大,据此分析解答.
解答:
解:加水稀释促进NH3?H2O电离,溶液中c(NH4+)、c(OH-)、c(NH3.H2O)都减小,c(H+)增大,
A.促进电离,则溶液中n(NH4+)增大、n(NH3.H2O)减小,所以
比值增大,故A错误;
B.加水稀释促进NH3?H2O电离,溶液中N(OH-) 增大,故B错误;
C.加水稀释促进NH3?H2O电离,溶液中n(OH-)增大、n(NH3.H2O)减小,则
比值增大,故C错误;
D.促进电离,则溶液中n(NH4+)增大,但溶液中铵根离子增大的量小于溶液体积增大的量,所以c(NH4+)减小,故D正确;
故选D.
A.促进电离,则溶液中n(NH4+)增大、n(NH3.H2O)减小,所以
| c(NH4+) |
| c(NH3?H2O) |
B.加水稀释促进NH3?H2O电离,溶液中N(OH-) 增大,故B错误;
C.加水稀释促进NH3?H2O电离,溶液中n(OH-)增大、n(NH3.H2O)减小,则
| c(OH-) |
| c(NH3?H2O) |
D.促进电离,则溶液中n(NH4+)增大,但溶液中铵根离子增大的量小于溶液体积增大的量,所以c(NH4+)减小,故D正确;
故选D.
点评:本题考查了弱电解质的电离,明确弱电解质的电离特点是解本题关键,知道稀释过程中粒子浓度任何变化,易错选项是D,虽然促进电离,但c(NH4+)、c(OH-) 都减小,为易错点.

练习册系列答案
相关题目
下列离子方程式书写正确的是( )
| A、泡沫灭火器的灭火原理是2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ |
| B、向硫酸铝中加入过量氨水Al3++4NH3?H2O═AlO2-+4NH4++2H2O |
| C、向硫酸亚铁酸性溶液中加入过氧化氢4Fe2++H2O2+2H+═4Fe3++2H2O |
| D、向明矾溶液中逐滴加入氢氧化钡溶液至硫酸根离子刚好沉淀完全2Ba2++4OH-+Al3++2SO42-═2BaSO4↓+AlO2-+2H2O |
 如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M g/mol,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )
如图是氯化铯晶体的晶胞,已知晶体中2个最近的Cl-离子核间距为a cm,氯化铯的摩尔质量为M g/mol,NA为阿伏加德罗常数,则氯化铯晶体的密度为( )A、
| ||
B、
| ||
C、
| ||
D、
|
下列物质变化的现象,不可以通过分子间作用力解释的是( )
| A、HF、H2O的沸点比HCl、H2S的沸点高很多 |
| B、正戊烷的沸点比新戊烷的沸点高 |
| C、H2O的沸点比FH的沸点高 |
| D、HF、HCl、HBr、HI的稳定性逐渐减弱 |
下列有关NA的说法不正确的是( )
| A、标况下1mol HF 的体积约为22.4 L |
| B、1.44g CaO2中所含阴离子数目为0.02NA |
| C、标况下4.48L CO2中含有的共用电子对数目为0.8NA |
| D、标准状况下,11.2L Cl2通入足量的石灰乳中制备漂白粉,转移的电子数为0.5NA |
将足量Cu和含2mol溶质的浓H2SO4在加热条件下充分反应,产生SO2在标况下的体积为( )
| A、22.4L |
| B、44.8L |
| C、小于22.4L |
| D、小于44.8L |
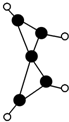 科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( )
科学家最近在-100℃的低温下合成了一种烃X,红外光谱和核磁共振氢谱表明其分子中的氢原子所处的化学环境没有区别,根据分析,绘制了该分子的球棍模型如图所示,下列说法中不正确的是( )| A、该分子的分子式为C5H4 |
| B、该分子中碳原子的化学环境有2种 |
| C、1mol X在一定条件下可与2mol H2发生反应 |
| D、该分子中只有C-C键,没有C═C键 |
下列与化学概念有关的说法正确的是( )
| A、化合反应均为氧化还原反应 |
| B、催化剂能改变可逆反应达到平衡的时间 |
| C、金属氧化物均为碱性氧化物 |
| D、石油是混合物,其分馏产品汽油为纯净物 |
