题目内容
按热稳定性递增的顺序排列的一组氢化物是( )
| A、H2S、HCl、HBr |
| B、H2S、HCl、HF |
| C、H2O、H2S、HCl |
| D、CH4、NH3、PH3 |
考点:非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:同一周期元素,元素的非金属性随着原子序数增大而增强,同一主族元素,元素的非金属性随着原子序数增大而减弱,元素的非金属性越强,其气态氢化物越稳定,据此分析解答.
解答:
解:A.非金属性Cl>Br>S,所以气态氢化物的稳定性:H2S<HBr<HCl,故A错误;
B.非金属性S<Cl<F,所以气态氢化物的稳定性H2S<HCl<HF,故B正确;
C.非金属性S<O,所以气态氢化物的稳定性H2S<H2O,故C错误;
D.非金属性P<N,所以气态氢化物的稳定性PH3<NH3,故D错误;
故选B.
B.非金属性S<Cl<F,所以气态氢化物的稳定性H2S<HCl<HF,故B正确;
C.非金属性S<O,所以气态氢化物的稳定性H2S<H2O,故C错误;
D.非金属性P<N,所以气态氢化物的稳定性PH3<NH3,故D错误;
故选B.
点评:本题考查非金属性强弱判断,明确非金属性强弱与其气态氢化物稳定性强弱关系是解本题关键,熟练掌握同一周期、同一主族非金属性强弱规律,题目难度不大.

练习册系列答案
相关题目
海水是重要的资源,可以制备一系列物质如图.下列说法正确的是( )
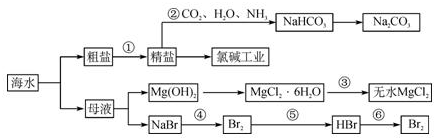

| A、步骤④、⑤、⑥反应中,溴元素均被氧化 | ||
B、除去粗盐中的S
| ||
| C、步骤②中,应先通CO2,再通NH3 | ||
| D、步骤③可将MgCl2?6H2O晶体在空气中直接加热脱水 |
在我国文明发展过程中,最早较广泛使用的金属是( )
| A、铜 | B、铁 | C、铝 | D、铅 |
摩尔质量为M g/mol的某物质在20℃时的溶解度为Sg/100g水,其20℃的饱和溶液的密度为d g/mL,其物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列变化规律正确的是( )
| A、感光性:AgF<AgCl<AgBr<AgI |
| B、还原性:F-<Cl-<Br-<I- |
| C、酸性:HF>HBr>HCl>HI |
| D、离子半径:F->Br->Cl->I- |
下列叙述中正确的是( )
| A、第三周期元素的离子半径从左到右依次减小 |
| B、HCl、PCl3、N2、CO2分子中所有原子都满足最外层8电子的结构 |
| C、晶体内可以不存在化学键,也可以同时存在离子键、极性键和非极性键 |
| D、若某离子化合物X2Y3中X3+和Y2-的电子层结构相同,则X、Y两元素的原子序数之差一定为6 |
下列物质中不能通过置换反应生成的是( )
| A、Al2O3 |
| B、F2 |
| C、Fe3O4 |
| D、C |