题目内容
某恒温容器用固定隔板隔成甲、乙两容器,如图所示,在甲、乙两容器中都充入1 mol A和2 mol B,反应3A(g)+B(g) xC(g)达到平衡后,甲、乙两容器中A物质的浓度比为5:3,甲、乙两容器中C的体积分数大小为 ( )
xC(g)达到平衡后,甲、乙两容器中A物质的浓度比为5:3,甲、乙两容器中C的体积分数大小为 ( )
| A.甲>乙 | B.甲<乙 | C.甲=乙 | D.无法确定 |
A
解析

练习册系列答案
相关题目
在2L恒容密闭容器中充入2 mol X和1mol Y发生反应:2X(g)+Y(g) 3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
3Z(g)△H<0,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断正确的是
| A.升高温度,平衡常数增大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.Q点时,Y的转化率最大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是( )
| A.Cu能与浓硝酸反应,而不与浓盐酸反应 |
| B.Cu与浓硝酸反应比与稀硝酸反应快 |
| C.N2与O2在常温、常压下不反应,放电时可反应 |
| D.Cu与浓硫酸反应,而不与稀硫酸反应 |
N2+3H2 2NH3反应达到平衡时的说法不正确的是( )。
2NH3反应达到平衡时的说法不正确的是( )。
| A.平衡体系中氮气、氢气、氨的物质的量保持不变 |
| B.平衡体系中氮气、氢气、氨的浓度保持不变 |
| C.单位时间内生成的氨和分解的氨物质的量相同 |
| D.单位时间内消耗的氮气和氢气与生成的氨气物质的量相同 |
等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到下图,则曲线a、b、c、d所对应的实验组别可能是( )。
| 组别 | c(HCl)/mol·L-1 | 温度/℃ | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 块状 |
| 4 | 2.5 | 50 | 粉末状 |
A.4
 3
3 2
2 1 B.1
1 B.1 2
2 3
3 4 C.3
4 C.3 4
4 2
2 1 D.1
1 D.1 2
2 4
4 3
3 在体积为V L的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g) 2HBr(g) ΔH<0。当温度分别为T1,T2,平衡时,H2的体积分数与Br2(g)的物质的量的变化关系如图所示。下列说法不正确的是 ( )
2HBr(g) ΔH<0。当温度分别为T1,T2,平衡时,H2的体积分数与Br2(g)的物质的量的变化关系如图所示。下列说法不正确的是 ( )
| A.由图可知:T1>T2 |
| B.a、b两点的反应速率:b>a |
| C.为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法 |
| D.T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增大 |
反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率可表示为
4NO(g)+6H2O(g)在10 L密闭容器中进行,半分钟后,水蒸气的物质的量增加了0.45 mol,则此反应的平均速率可表示为
A. (NH3)=0.010 0 mol/(L·s) (NH3)=0.010 0 mol/(L·s) |
B. (O2)=0.001 0 mol/(L·s) (O2)=0.001 0 mol/(L·s) |
C. (NO)=0.001 0 mol/(L·s) (NO)=0.001 0 mol/(L·s) |
D. (H2O)=0.045 mol/(L·s) (H2O)=0.045 mol/(L·s) |

 2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)
2A(g) + B(g)该反应的平衡常数表达式为K=c(A)2·c(B)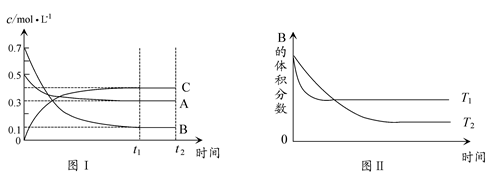
 2C(g) ΔH>0
2C(g) ΔH>0