题目内容
18.一定条件下,在恒温恒容的密闭容器中充入一定量的A和B,发生反应:2A(g)+B(g)?3C(g)+D(s),经测定,0~4s时间段内,v(A)=0.10mol•L-1•s-1,则8s末时C的浓度为( )| A. | 大于1.2mol•L-1 | B. | 小于1.2mol•L-1 | C. | 等于1.2mol•L-1 | D. | 不能确定 |
分析 恒温恒容条件下,气体反应速率与物质的物质的量浓度成正比,随着反应的进行,正反应速率逐渐减小,0~4s时间段内,v(A)=0.10mol•L-1•s-1,假设反应是匀速进行的,则8s末时,参加反应的△c(A)=0.10mol•L-1•s-1×8s=0.80mol/L,同一化学反应中同一时间段内,参加反应的各物质的物质的量浓度变化量之比等于其计量数之比,则8s末时△c(C)=$\frac{3}{2}$△c(A)=$\frac{3}{2}$×0.80mol/L=1.20mol/L,实际上,反应速率是随着反应进行而降低的,据此计算.
解答 解:恒温恒容条件下,气体反应速率与物质的物质的量浓度成正比,随着反应的进行,正反应速率逐渐减小,0~4s时间段内,v(A)=0.10mol•L-1•s-1,假设反应是匀速进行的,则8s末时,参加反应的△c(A)=0.10mol•L-1•s-1×8s=0.80mol/L,同一化学反应中同一时间段内,参加反应的各物质的物质的量浓度变化量之比等于其计量数之比,则8s末时△c(C)=$\frac{3}{2}$△c(A)=$\frac{3}{2}$×0.80mol/L=1.20mol/L,实际上,反应速率是随着反应进行而降低的,则8s末△c(C)小于1.2mol•L-1,故选B.
点评 本题以化学平衡建立过程为载体考查化学反应速率有关计算,明确反应速率与物质的量浓度关系是解本题关键,注意:化学反应速率不是匀速进行的,在到达平衡状态前正反应速率是逐渐减小的,为易错点.

练习册系列答案
 小学能力测试卷系列答案
小学能力测试卷系列答案
相关题目
9.下列实验设计或实验操作中,正确的是( )
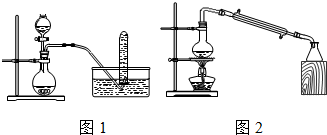

| A. | 铜与浓硝酸反应制取NO2可采用图1装置: | |
| B. | 图2实验装置设计正确,该装置可实现石油的分馏 | |
| C. | 分离乙酸和乙醇溶液:不能用分液漏斗进行分离 | |
| D. | 制乙酸乙酯时,把乙醇和乙酸依次加入浓硫酸中 |
13.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 28g乙烯(C2H4)中含有的π键数与13g乙炔(C2H2)中含有的π键数一样多 | |
| B. | 通过MnO2催化使H2O2分解,产生16g O2时转移电子数为2NA | |
| C. | 2.24L NH3中含共价键数目一定为0.3NA | |
| D. | 5.6g Fe投入100mL 3.5mol•L-1稀硝酸中,充分反应,转移电子总数为0.3 NA |
3.在同温同压下,等体积的四瓶混合气体:(1)N2;(2)O2;(3)CO2;(4)NO2,气体密度由大到小的排序正确的是( )
| A. | (1)>(2)>(3)>(4) | B. | (2)>(4)>(3)>(1) | C. | (3)>(4)>(2)>(1) | D. | (4)>(3)>(2)>(1) |
10.m g相对分子质量为M的二元强碱溶于水配制V L溶液,该溶液中c(OH-)为( )
| A. | $\frac{m}{MV}$mol•L-1 | B. | $\frac{2m}{MV}$mol•L-1 | C. | $\frac{m}{2MV}$mol•L-1 | D. | $\frac{2M}{mV}$mol•L-1 |
7.下列有关气体摩尔体积的描述中正确的是( )
| A. | 在一定温度和压强下,单位物质的量的气体所占的体积就是气体摩尔体积 | |
| B. | 在0℃,1标准大气压下的气体摩尔体积约为22.4L | |
| C. | 标准状况下,1mol酒精的体积约为22.4L | |
| D. | 相同物质的量的气体,其体积也相同 |
8.用NA表示阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 在标准状况下,2.24L苯中含有0.6NA个碳原子 | |
| B. | 1L pH=1的硫酸溶液中含有0.2NA个氢离子 | |
| C. | 1L 1mol•L-1的FeCl3溶液中,含有铁离子的数目为NA | |
| D. | t时,1L pH=6的纯水中,含有10-6NA个OH- |