题目内容
用右图所示装置进行实验,将少量液体甲逐滴加入到固体乙中,试管中试剂为丙,则下表中现象与结论均正确的是

选项 甲 乙 丙 试管中现象 结论
A 稀硫酸 亚硫酸钠 溴水 橙色褪去 SO2具有漂白性
B 饱和食盐水 电石 酸性 KMnO4溶液 紫色褪去 乙炔可发生氧化反应
C 醋酸 碳酸钠 BaCl2溶液 变浑浊 醋酸酸性强于碳酸
D 浓氨水 生石灰 AgNO3溶液 无明显现象 NH3与 AgNO3溶液不反应
【答案】
B
【解析】
试题分析:A项因为发生氧化还原反应而使溴水褪色,错误;C项BaCl2溶液中没有明显现象,错误;D项AgNO3溶液中通入氨气会出现白色沉淀,氨气过量溶液又变澄清,错误。
考点:简单实验。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
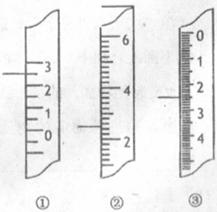 (4分).(1)温度计常用来监测或控制化学实验的温度。
(4分).(1)温度计常用来监测或控制化学实验的温度。 C.③是滴定管,读数为3.5 mL
C.③是滴定管,读数为3.5 mL 现将6.0molCO2和8.0molH2充入2L的密闭容器中,测得H2的物质的量(n)随时间变化如下图所示(实线)。
现将6.0molCO2和8.0molH2充入2L的密闭容器中,测得H2的物质的量(n)随时间变化如下图所示(实线)。
 ③以此电池做电源,在实验室中模拟铝制品表面
③以此电池做电源,在实验室中模拟铝制品表面