题目内容
7.X、Y、Z常见的短周期元素可以形成XY2、Z2Y、XY3、Z2Y2、Z2X等化合物.已知Y的离子和Z的离子有相同的电子层结构,X离子比Y离子多一个电子层.试回答:(1)写出X、Y、Z种元素的符号和名称:S或硫;O或氧;Na或钠
(2)分析Z2Y2中含有的化学键类型:离子键和非极性键
(3)写出Z2Y2与二氧化碳反应的方程式:2Na2O2+2CO2=2Na2CO3+O2
(4)用电子式表示X和Z两种素形成化合物的过程:
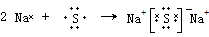 .
.
分析 由Z2Y、Z2Y2可推测是H2O、H2O2或Na2O、Na2O2,又因为Y离子和Z离子具有相同的电子层结构,所以只能是Na2O、Na2O2,由此知Z为Na,Y为O,由于XY2、XY3,可知X可形成?+4、+6价的化合物,且X离子比Y离子多1个电子层,X只能是S,结合对应物质的性质以及题目要求解答该题.
解答 解:由Z2Y、Z2Y2可推测是H2O、H2O2或Na2O、Na2O2,又因为Y离子和Z离子具有相同的电子层结构,所以只能是Na2O、Na2O2,由此知Z为Na,Y为O,由于XY2、XY3,可知X可形成?+4、+6价的化合物,且X离子比Y离子多1个电子层,X只能是S,
(1)X为S或硫,Y为O或氧,Z为Na或钠,故答案为:S或硫;O或氧;Na或钠;
(2)Z2Y2为Na2O2,钠离子与过氧根离子形成离子键,过氧根中形成O-O非极性键,故答案为:离子键和非极性键;
(3)Z2Y2为Na2O2,与二氧化碳反应的方程式为2Na2O2+2CO2=2Na2CO3+O2,故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)X和Z两种素形成化合物为硫化钠,形成过程为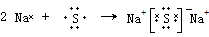
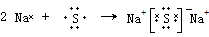
点评 本题考查了位置、结构与性质关系的综合应用,题目难度中等,正确推断各元素名称为解答关键,注意熟练掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
17.某含氮有机物C4H9NO2有多种同分异构体,其中属于氨基酸的同分异构体数目为( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
18.正确掌握化学用语是学好化学的基础.下列化学用语正确的是( )
| A. | 甲基的电子式  | B. | 乙烯的结构简式 CH2CH2 | ||
| C. | 聚丙烯的结构简  | D. | 葡萄糖的实验式(最简式)CH2O |
2.现有一些物质含有少量杂质(括号中未杂质),下列方法不能除去杂质的是( )
| A. | 苯(苯酚):滴入适量的氢氧化钠溶液,振荡,分液 | |
| B. | 苯酚钠(氯化钠):通入过量的CO2,过滤后在沉淀中加入烧碱溶液 | |
| C. | 乙酸乙酯(乙醇):加入适量饱和碳酸钠溶液,振荡,分液 | |
| D. | 硬脂酸钠(甘油\烧碱和水):加入食盐细粒充分搅拌,静置后过滤 |
12.下列依据相关实验得出的结论正确的是( )
| A. | 用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,则该溶液一定是钠盐溶液 | |
| B. | 测定同温同浓度的Na2CO3和Na2SiO3溶液的pH,发现Na2SiO3溶液的pH大,则碳的非金属性强于硅 | |
| C. | 淀粉与稀硫酸混合加热一段时间,滴加银氨溶液并水浴加热,无银镜出现,则淀粉没有水解 | |
| D. | 向浓度均为0.1 mol•L-1 NaCl和NaI混合溶液中滴加少量稀AgNO3溶液,出现黄色沉淀,说明Ksp(AgCl)>Ksp(AgI) |
2.NA表示阿佛加德罗常数,下列说法正确的是( )
| A. | 1mol 任何气体的体积都约是22.4L | |
| B. | 18gNH4+含有电子数为10NA | |
| C. | NA个H2SO4分子的质量与H3PO4的摩尔质量在数值上相等 | |
| D. | 标准状况下,相同体积的O2、HCl、H2O含有的分子数相同 |
19.若不断地升高温度,实现“水→水蒸气→氧气和氢气→氧原子和氢原子”的变化.在变化的各阶段被破坏的粒子间的主要相互作用依次是( )
| A. | 氢键;分子间作用力;非极性键 | B. | 氢键;极性键;分子间作用力 | ||
| C. | 氢键;极性键; 非极性键 | D. | 分子间作用力;氢键;非极性键 |
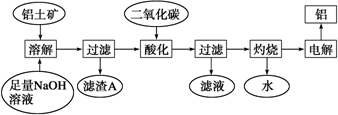
 图为实验室制取某有机物的装置图,试通过已学知识回答下列问题:
图为实验室制取某有机物的装置图,试通过已学知识回答下列问题: .
.