题目内容
【题目】下列实验设计能够成功的是( )
A.检验亚硫酸钠试样是否变质:试样 ![]() 滴加
滴加 ![]() 白色沉淀滴加
白色沉淀滴加 ![]() 沉淀不溶解﹣→说明试样已变质
沉淀不溶解﹣→说明试样已变质
B.除去粗盐中硫酸钙杂质:粗盐 ![]() 足量
足量 ![]() 足量
足量 ![]() 溶液
溶液 ![]() 滤液中
滤液中 ![]() 盐酸
盐酸 ![]() 精盐
精盐
C.检验某溶液中是否含有Fe2+试样 ![]() 溶液颜色无变化
溶液颜色无变化 ![]() 溶液变红色﹣→溶液中含有Fe2+
溶液变红色﹣→溶液中含有Fe2+
D.证明酸性条件H2O2的氧化性比I2强:NaI溶液30% ![]() 稀硝酸
稀硝酸 ![]() 溶液变蓝色﹣→氧化性:H2O2>I2
溶液变蓝色﹣→氧化性:H2O2>I2
【答案】C
【解析】解:A.若变质生成硫酸钠,应先加盐酸,排除亚硫酸根离子的干扰,再加氯化钡检验硫酸钠的存在,故A错误; B.应先加氯化钡,再加碳酸钠,然后过滤后再加盐酸可实现除杂,选项B中钡离子不能除去,故B错误;
C.亚铁离子遇KSCN溶液不变色,滴加氯水后亚铁离子被氧化生成铁离子遇KSCN溶液变色,可证明溶液中含有Fe2+ , 故C正确;
D.硝酸具有强氧化性,可氧化碘离子,不能说明H2O2的氧化性比I2强,应选盐酸,故D错误;
故选C.
A.应先加盐酸,排除亚硫酸根离子的干扰;
B.应先加氯化钡,再加碳酸钠;
C.亚铁离子遇KSCN溶液不变色,亚铁离子被氧化生成铁离子遇KSCN溶液变色;
D.硝酸具有强氧化性,可氧化碘离子.

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl22H20),为制取纯净的CuCl22H20,首先将其制成水溶液,然后按如图步骤进行提纯: 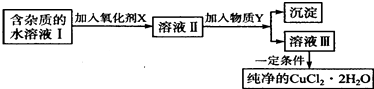
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见表:
Fe3+ | Fe2+ | Cu2+ | |
氢氧化物开始沉淀时的PH | 1.9 | 7.0 | 4.7 |
氢氧化物完全沉淀时的PH | 3.2 | 9.0 | 6.7 |
请回答下列问题.
(1)最适合作氧化剂X的是 .
A.K2Cr207
B.NaCl0
C.H202
D.KMn04
(2)加入的物质Y是 .
A.CuO
B.NaOH
C.Cu2(OH)2CO3
D.NH3
(3)由溶液Ⅲ获得CuCl22H2O,需要经过、、过滤操作.
(4)测定溶液Ⅰ中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4溶液应使用(“酸式”或“碱式”)滴定管.反应的化学方程式: .
【题目】铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl22H20),为制取纯净的CuCl22H20,首先将其制成水溶液,然后按如图步骤进行提纯: 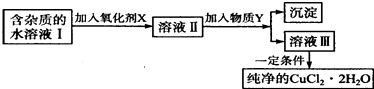
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见表:
Fe3+ | Fe2+ | Cu2+ | |
氢氧化物开始沉淀时的PH | 1.9 | 7.0 | 4.7 |
氢氧化物完全沉淀时的PH | 3.2 | 9.0 | 6.7 |
请回答下列问题.
(1)最适合作氧化剂X的是 .
A.K2Cr207
B.NaCl0
C.H202
D.KMn04
(2)加入的物质Y是 .
A.CuO
B.NaOH
C.Cu2(OH)2CO3
D.NH3
(3)由溶液Ⅲ获得CuCl22H2O,需要经过、、过滤操作.
(4)测定溶液Ⅰ中Fe2+的浓度,可用KMnO4标准溶液滴定,取用KMnO4溶液应使用(“酸式”或“碱式”)滴定管.反应的化学方程式: .