题目内容
(1)若甲是由短周期元素形成的单质,并且该元素的原子最外电子层上的电子数为其内层电子层数的二分之一,则甲元素的原子结构示意图为____________,甲与水反应的离子方程式为_________________;
(2)乙为甲的稳定的氧化物,写出乙在与水反应中氧化剂的电子式____________;19.5g乙与足量的水反应转移电子的物质的量为____________mol;
(3)丙为地壳中金属元素含量排位第二的元素形成的单质,写出它与水蒸气反应的化学方程式________________________;在实验室里,配制丙的高价氯化物溶液时要加入一定量的盐酸,解释原因并写出离子反应方程式:________________________;
(4)丁是由两种均为10个电子的微粒组成的化合物,它与碱反应能生成一种有刺激性气味的气体X,X分子中也含有10个电子,则丁属于____________类型的晶体,从综合效益角度出发,在工业上生产X时,既要增大单位时间内X产量,又要提高X的产率,可采取的措施是(填写下列合理选项的序数)
_______________。
①减压 ②加压 ③升温 ④降温 ⑤适宜的温度和压强 ⑥加催化剂
⑦及时从平衡体系中分离出X ⑧分离出X后的原料气循环使用并补充原料
 ;2Na+2H2O==2Na++2OH-+ H2↑
;2Na+2H2O==2Na++2OH-+ H2↑(2)
 ;0.25mol
;0.25mol (3)3Fe+4H2O(g)
 Fe3O4+4H2;Fe3++3H2O
Fe3O4+4H2;Fe3++3H2O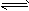 Fe(OH)3↓+3H+加入盐酸可使该平衡向左移动,从而抑制Fe3+的水解
Fe(OH)3↓+3H+加入盐酸可使该平衡向左移动,从而抑制Fe3+的水解(4)离子晶体;⑤⑥⑦⑧

| 甲 | 乙 | 丙 | 丁 |
化合物中各元素原子个数比 | A∶C | B∶A | D∶E | B∶E |
1∶1 | 1∶2 | 1∶3 | 1∶4 |
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和,B原子最外层电子数比其次外层电子数多2个。在周期表中,C是E的邻族元素,化学性质活泼,D和E则位于同一周期,D和E的原子序数之和为30。
(1)写出元素符号:A___________,B___________,C___________,D___________,E___________。
(2)向甲的水溶液中加入MnO2,反应的化学方程式是____________________________。
(3)已知乙的式量小于甲,在实验室中常用什么方法制得乙:______________________
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会迅速产生大量气体和难溶物,有关离子方程式为______________________。
(5)向3 mL 1 mol·L-1KI溶液中依次注入下列试剂:①1 mL 5 mol·L-1盐酸;②0.5 mL 30%甲溶液;③1 mL丁。经充分振荡后静置,可得到紫色溶液,这种紫色溶液是___________。
(9分)A、B、C、D、E五种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的不同周期邻族元素;D和E的原子序数之和为30。它们两两形成的化合物为甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:(用元素符号作答)
|
| 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
(1)写出A~E的元素符号
A: B: C: D: E:
(2)向甲的水溶液中加入MnO2,氧化产物是 。
(3)已知有机物乙的分子为平面结构,碳氢键键角为120°,实验室制取乙的化学方程式为:
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式是:

 。
。