题目内容
甲、乙、丙、丁四种物质之间具有如右转化关系: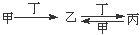 。
。
请回答下列问题:
(1)若乙为两性不溶物,则丙转化为乙的离子方程式为 ;
(2)若丙为形成酸雨的主要物质,则甲的化学式 ,乙能与热的NaOH溶液反应,产物中元素的最高价态为+4,写出该反应的离子方程式为 ;
(3)若丙中含有目前人类使用最广泛的金属元素,且乙转化成丙为化合反应,则将丙溶液蒸发、灼烧得到的物质是 ,除去丙溶液中少量乙的方法是 (用化学方程式表示),如何检验乙溶液中的丙,请设计实验方案 。
(1)Al3++3AlO2-+6H2O=4Al(OH)3 ↓ ;
(2)H2S ,3S+6OH- = 2S2-+SO3 2- + 3H2O ;
(3)Fe2O3(1分) , 2FeCl3+Fe=3FeCl2 ;取少量乙(FeCl3)溶液于试管中,滴加酸性高锰酸钾溶液,若高锰酸钾溶液褪色,则乙溶液中含有丙(FeCl2 ) (其他合理答案均可) 。
【解析】
试题分析:(1)乙为两性不溶物,即为氢氧化铝,则丙为偏铝酸钠,相关离子方程式:Al3++3AlO2-+6H2O=4Al(OH)3
↓ ;(2)若丙为形成酸雨的主要物质,即丙为二氧化硫,则甲为硫化氢,乙为硫单质;硫与热的NaOH溶液反应,3S+6OH- =
2S2-+SO3 2- + 3H2O;(3)目前人类使用最广泛的金属元素为铁,符合条件的变化:Cl2 FeCl3
FeCl3 FeCl2
,亚铁离子具有还原性,加热过程中被氧化为氯化铁,氯化铁溶液蒸发促进三价铁离子水解,氯化氢属于挥发性酸,氯化氢挥发掉,得到氢氧化铁沉淀,灼烧得到氧化铁固体;除去氯化铁溶液中的氯化亚铁,加足量的金属铁即可,相关化学方程式:2FeCl3+Fe=3FeCl2 ;检验亚铁离子办法,取少量乙(FeCl3)溶液于试管中,滴加酸性高锰酸钾溶液,若高锰酸钾溶液褪色,则乙溶液中含有丙(FeCl2 ) 。
FeCl2
,亚铁离子具有还原性,加热过程中被氧化为氯化铁,氯化铁溶液蒸发促进三价铁离子水解,氯化氢属于挥发性酸,氯化氢挥发掉,得到氢氧化铁沉淀,灼烧得到氧化铁固体;除去氯化铁溶液中的氯化亚铁,加足量的金属铁即可,相关化学方程式:2FeCl3+Fe=3FeCl2 ;检验亚铁离子办法,取少量乙(FeCl3)溶液于试管中,滴加酸性高锰酸钾溶液,若高锰酸钾溶液褪色,则乙溶液中含有丙(FeCl2 ) 。
考点:本题为框图型物质推断题,完成此类题目,可以依据题干提供的信息,结合框图,找准解题的突破口,直接得出物质的化学式,然后顺推或逆推或由两边向中间推得出其他物质的化学式。

 名校课堂系列答案
名校课堂系列答案
| 甲 | 乙 | 丙 | 丁 |
化合物中各元素原子个数比 | A∶C | B∶A | D∶E | B∶E |
1∶1 | 1∶2 | 1∶3 | 1∶4 |
其中A、B两种原子的核电荷数之差等于它们的原子最外层电子数之和,B原子最外层电子数比其次外层电子数多2个。在周期表中,C是E的邻族元素,化学性质活泼,D和E则位于同一周期,D和E的原子序数之和为30。
(1)写出元素符号:A___________,B___________,C___________,D___________,E___________。
(2)向甲的水溶液中加入MnO2,反应的化学方程式是____________________________。
(3)已知乙的式量小于甲,在实验室中常用什么方法制得乙:______________________
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会迅速产生大量气体和难溶物,有关离子方程式为______________________。
(5)向3 mL 1 mol·L-1KI溶液中依次注入下列试剂:①1 mL 5 mol·L-1盐酸;②0.5 mL 30%甲溶液;③1 mL丁。经充分振荡后静置,可得到紫色溶液,这种紫色溶液是___________。
(9分)A、B、C、D、E五种短周期元素,已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;在元素周期表中,C是E的不同周期邻族元素;D和E的原子序数之和为30。它们两两形成的化合物为甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:(用元素符号作答)
|
| 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素原子个数比 | A:C=1:1 | B:A=1:2 | D:E=1:3 | B:E=1:4 |
(1)写出A~E的元素符号
A: B: C: D: E:
(2)向甲的水溶液中加入MnO2,氧化产物是 。
(3)已知有机物乙的分子为平面结构,碳氢键键角为120°,实验室制取乙的化学方程式为:
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量气体和难溶物,有关离子方程式是: