题目内容
现有300mL MgCl2溶液,密度为1.18g/cm3,其中Mg2+的质量分数为5.1%.
(1)求该溶液中氯离子的物质的量.(结果保留1位小数)
(2)向其中加入200mL 5mol/L NaOH溶液,充分反应后,求溶液中Mg2+的物质的量浓度.(溶液混合过程中体积变化忽略不计)
解:(1)m(Mg2+)=m(溶液)×ω(Mg2+)=300mL×1.18g/mL×5.1%=354×5.1%g,
故溶液中n(Mg2+)= =
= mol,
mol,
根据电荷守恒,溶液中n(Cl-)=2n(Mg2+)=2× mol=1.5mol,
mol=1.5mol,
答:该溶液中氯离子的物质的量为1.5mol;
(2)混合后溶液中n(Cl-)= =3mol/L,
=3mol/L,
反应后溶液中钠离子的物质的量不变,则:500mL×c(Na+)=200mL×5mol/L,解得c(Na+)=2mol/L,
由题意可知,混合后溶液为氯化镁与氯化钠溶液,根据电荷守恒有c(Cl-)=2c(Mg2+)+c(Na+),即:
3mol/L=2c(Mg2+)+2mol/L,
解得c(Mg2+)=0.5mol/L,
答:溶液中Mg2+的物质的量浓度为0.5mol/L.
分析:(1)根据m(Mg2+)=m(溶液)×ω(Mg2+)计算溶液中镁离子质量,再根据n= 计算n(Mg2+),根据电荷守恒,溶液中n(Cl-)=2n(Mg2+),据此计算;
计算n(Mg2+),根据电荷守恒,溶液中n(Cl-)=2n(Mg2+),据此计算;
(2)由题意可知,混合后溶液为氯化镁与氯化钠溶液,根据电荷守恒有c(Cl-)=2c(Mg2+)+c(Na+),根据稀释定律计算混合后溶液中c′(Cl-)、c(Na+),据此计算.
点评:本题考查物质的量浓度的有关计算,难度中等,(2)中若按常规解法进行比较复杂,注意利用电荷守恒进行的计算.
故溶液中n(Mg2+)=
 =
= mol,
mol,根据电荷守恒,溶液中n(Cl-)=2n(Mg2+)=2×
 mol=1.5mol,
mol=1.5mol,答:该溶液中氯离子的物质的量为1.5mol;
(2)混合后溶液中n(Cl-)=
 =3mol/L,
=3mol/L,反应后溶液中钠离子的物质的量不变,则:500mL×c(Na+)=200mL×5mol/L,解得c(Na+)=2mol/L,
由题意可知,混合后溶液为氯化镁与氯化钠溶液,根据电荷守恒有c(Cl-)=2c(Mg2+)+c(Na+),即:
3mol/L=2c(Mg2+)+2mol/L,
解得c(Mg2+)=0.5mol/L,
答:溶液中Mg2+的物质的量浓度为0.5mol/L.
分析:(1)根据m(Mg2+)=m(溶液)×ω(Mg2+)计算溶液中镁离子质量,再根据n=
 计算n(Mg2+),根据电荷守恒,溶液中n(Cl-)=2n(Mg2+),据此计算;
计算n(Mg2+),根据电荷守恒,溶液中n(Cl-)=2n(Mg2+),据此计算;(2)由题意可知,混合后溶液为氯化镁与氯化钠溶液,根据电荷守恒有c(Cl-)=2c(Mg2+)+c(Na+),根据稀释定律计算混合后溶液中c′(Cl-)、c(Na+),据此计算.
点评:本题考查物质的量浓度的有关计算,难度中等,(2)中若按常规解法进行比较复杂,注意利用电荷守恒进行的计算.

练习册系列答案
相关题目




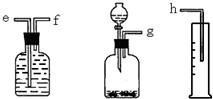 (1)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合:
(1)测定Na2O和Na的混合物中金属钠的质量分数可用下图所示的几套仪器组合: