题目内容
下列各组离子在指定溶液中能大量共存的是
A.在无色溶液中: Na+、Cu2+、NO3- 、MnO4-
B.在含有HCO3-的溶液中:H+、K+、SO42-、Cl-
C.PH=1的溶液中:Na+、 K+、AlO2-、SO42-
D.常温下,水电离的c(H+)=10-12mol·L-1的溶液中:K+、Ba2+、NO3-、Cl-
D
【解析】
试题分析:A中MnO4-是紫色离子,A错;B中HCO3-和H+会发生反应不能大量共存,B错;C、 PH=1是酸性溶液,AlO2-不能存在于酸性溶液中,错,选D.
考点:离子的大量共存问题。

 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案(10分) CO2和CH4是两种重要的温室气体,通过CH4和CO2反应来制造更高价值的化学品是目前的研究目标。
(1)250 ℃时,以镍合金为催化剂,向体积为4 L的密闭容器中通入6 mol CO2、6 mol CH4,发生如下反应:CO2(g)+CH4(g) 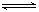 ?2CO(g)+2H2(g)。
?2CO(g)+2H2(g)。
平衡体系中各组分体积分数(某一成分物质的量占总气体物质的量的百分数)如下表:
物质 | CH4 | CO2 | CO | H2 |
体积分数 | 0.1 | 0.1 | 0.4 | 0.4 |
①此温度下该反应的平衡常数K=________。
②已知:CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
CO(g)+H2O(g)===CO2(g)+H2(g) ΔH=+2.8 kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH=-566.0 kJ·mol-1
反应CO2(g)+CH4(g) ===?2CO(g)+2H2(g) ΔH=________。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
①在不同温度下催化剂的催化效率与乙酸的生成速率如下图所示。250~300 ℃时,乙酸的生成速率减小的原因是__________________________________________________。

②将Cu2Al2O4溶解在稀硝酸中的离子方程式为_______________________________。
(3)以CO2为原料可以合成多种物质。
如合成聚碳酸酯。已知CO2的分子结构为O===C===O,它的“C===O”双键与乙烯的“C===C”双键一样,在一定条件下可发生加聚反应,聚碳酸酯是一种易降解的新型合成材料,它是由CO2加聚而成。写出聚碳酸酯的结构简式:______________________________________。

 2B(g) +C(g)
2B(g) +C(g)
 。则下列判断错误的是
。则下列判断错误的是