题目内容
10.恒温恒容密闭容器中,有可逆反应:A(s)+2B(g)?C(g)+D(g),当下列物理量不再改变时,不能表明反应已达到平衡状态的是( )| A. | A(s)的质量 | B. | 混合气体的密度 | ||
| C. | 混合气体的压强 | D. | 混合气的平均相对分子质量 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、A(s)的质量不变,说明正逆反应速率相等,达平衡状态,故A错误;
B、混合气体的密度,说明气体的质量不变,反应达平衡状态,故B错误;
C、两边计量数相等,所以混合气体的压强始终不变,故C正确;
D、混合气的平均相对分子质量,说明气体的质量不变反应达平衡状态,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.已知:①H2O(g)=H2O(l)△H1=-a kJ•mol-1
②C2H5OH(g)=C2H5OH(l)△H2=-b kJ•mol-1
③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=-c kJ•mol-1
根据盖斯定律判断:若使46g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为( )
②C2H5OH(g)=C2H5OH(l)△H2=-b kJ•mol-1
③C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g)△H3=-c kJ•mol-1
根据盖斯定律判断:若使46g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为( )
| A. | (b-a-c)kJ | B. | (3a-b+c )kJ | C. | (a-3b+c)kJ | D. | (b-3a-c)kJ |
1.近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(α羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为 ,下列说法错误的是( )
,下列说法错误的是( )
 ,下列说法错误的是( )
,下列说法错误的是( )| A. | 苹果酸在一定条件下能跟乙酸发生酯化反应 | |
| B. | 苹果酸在一定条件下能与金属钠反应 | |
| C. | 苹果酸在一定条件下能跟乙醇发生酯化反应 | |
| D. | 1 mol苹果酸与Na2CO3溶液反应最多消耗3 mol Na2CO3 |
18.下列说法错误的是( )
| A. | 抗酸药能中和胃里过多的盐酸,是一类治疗胃痛的药 | |
| B. | 碳酸镁、碳酸钡都能制成抗酸药物 | |
| C. | 青霉素过敏严重者会导致死亡,故用药前要进行皮肤敏感试验 | |
| D. | 青霉素是最重要的消炎药 |
5.在水中加入下列物质,可以抑制水电离的是( )
| A. | NaOH | B. | CuCl2 | C. | CH3COONa | D. | KNO3 |
15.一定条件下,可逆反应X(g)+3Y(g)?2Z(g),若X、Y、Z起始浓度分别为C1、C2、C3(均不为0);平衡时,X、Y、Z的浓度分别为0.2mol•L-1,0.6mol•L-1,0.16mol•L-1,则下列判断不合理的是( )
| A. | 若反应从正方向开始,X、Y的转化率可能不相等 | |
| B. | C1:C2=1:3 | |
| C. | 平衡时,X和Z的生成速率之比为1:2 | |
| D. | C2的取值范围为0<C2<0.84 mol•L-1 |
2.配制100mL 1.0mol•L-1Na2CO3溶液,下列操作正确的是( )
| A. | 称取28.6 g Na2CO3•10H2O,加入100 mL容量瓶中,加水溶解、定容 | |
| B. | 称取 28.6 g Na2CO3•10H2O,加入100 mL蒸馏水,搅拌、溶解 | |
| C. | 转移时将烧杯中溶液直接倒人容量瓶中 | |
| D. | 定容后,塞好瓶塞,反复倒转、摇匀 |
19.ABS合成树脂的结构可表示为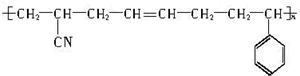 ,则合成该树脂的单体的种类和反应所属类型,正确的是( )
,则合成该树脂的单体的种类和反应所属类型,正确的是( )
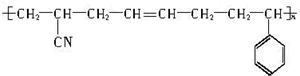 ,则合成该树脂的单体的种类和反应所属类型,正确的是( )
,则合成该树脂的单体的种类和反应所属类型,正确的是( )| A. | 1种,加聚反应 | B. | 2种,缩聚反应 | C. | 3种,加聚反应 | D. | 3种,缩聚反应 |
15.将已除去表面氧化膜的铝条和镁条按图示方式插入NaOH溶液中一段时间,下列叙述正确的是( )
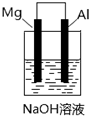

| A. | 该装置中镁条作负极 | |
| B. | 该装置中镁条上无气泡产生 | |
| C. | 该装置中电子从铝条经导线流向镁条 | |
| D. | 该装置中铝条表面产生气泡 |