题目内容
【题目】碳、氮元素及其化合物与生产、生活密切相关,回答下列问题。
(1)K3[Fe(CN)6]中Fe3+与CN-之间的作用为___,该化学键能够形成的原因是___。
(2)某有机物的结构简式为![]() 。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为___。
。该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序为___。
(3)乙二胺(H2NCH2CH2NH2)分子中氮原子杂化类型为___。
(4)NH4Cl中阳离子中心原子的价层电子对数为___,该物质中不含有___。
A.离子键 B.极性共价键 C.非极性共价键 D.配位键 E.σ键 F.π键
(5)NCl3的立体构型为___,其中心原子的杂化轨道类型为___。
【答案】配位键 Fe3+提供空轨道,CN-提供孤对电子,形成配位键 O>N>C sp3 4 CF 三角锥形 sp3
【解析】
(1)K3[Fe(CN)6]中Fe3+能提供空轨道,CN-能提供孤对电子,两者结合形成配位键;
(2)苯环上的碳原子为sp2杂化,其他碳原子均形成4个共价单键,为sp3杂化,氮原子形成3个共价单键,孤电子对数为1,故为sp3杂化,羟基氧原子形成2个共价单键,孤电子对数为2,故为sp3杂化,C、N、O位于同一周期,其电负性逐渐增大;
(3)乙二胺分子中每个氮原子形成3个共价单键,孤电子对数为1,价层电子对数为3+1=4,故为sp3杂化;
(4)![]() 中氮原子的价层电子对数为
中氮原子的价层电子对数为![]() ;
;![]() 与Cl-形成离子键,
与Cl-形成离子键,![]() 中氮原子与3个氢原子形成极性共价键,与剩余1个氢原子形成配位键,不存在非极性键和π键,故答案为:CF;
中氮原子与3个氢原子形成极性共价键,与剩余1个氢原子形成配位键,不存在非极性键和π键,故答案为:CF;
(5)NCl3分子中氮原子的价层电子对数为![]() ,孤电子对数为1,故为sp3杂化,分子的立体构型为三角锥形。
,孤电子对数为1,故为sp3杂化,分子的立体构型为三角锥形。

 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案【题目】现使用酸碱中和滴定法测定市售白醋的总酸量(g·100mL-1)。
Ⅰ.实验步骤
(1)用__(填仪器名称)量取10.00mL食用白醋,在烧杯中用水稀释后转移到100mL__(填仪器名称)中定容,摇匀即得待测白醋溶液。
(2)用酸式滴定管取待测白醋溶液20.00mL于锥形瓶中,向其中滴加2滴__作指示剂。
(3)读取盛装0.1000mol·L-1NaOH溶液的碱式滴定管的初始读数。如果液面位置如图所示,则此时的读数为__mL。
![]()
(4)滴定。当__时,停止滴定,并记录NaOH溶液的终读数。重复滴定3次。
Ⅱ.实验记录
滴定次数实验数据(mL) | 1 | 2 | 3 | 4 |
V(样品) | 20.00 | 20.00 | 20.00 | 20.00 |
V(NaOH)(消耗) | 15.95 | 15.00 | 15.05 | 14.95 |
Ⅲ.数据处理与讨论
(5)甲同学在处理数据时计算得:平均消耗的NaOH溶液的体积V=![]() mL=15.24mL。指出他的计算的不合理之处:__。
mL=15.24mL。指出他的计算的不合理之处:__。
按正确数据处理,可得c(市售白醋)=__mol·L-1;市售白醋总酸量=__g·100mL-1。
(6)在本实验的滴定过程中,下列操作会使实验结果偏大的是__(填写序号)。
a.碱式滴定管在滴定时未用标准NaOH溶液润洗
b.碱式滴定管的尖嘴在滴定前有气泡,滴定后气泡消失
c.锥形瓶中加入待测白醋溶液后,再加少量水
d.锥形瓶在滴定时剧烈摇动,有少量液体溅出
【题目】(1)常温下,向20mL0.05mol·L-1的某稀酸H2B溶液中滴入0.1mol·L-1氨水,溶液中由水电离出氢离子浓度随滴入氨水体积变化如图。回答下列问题
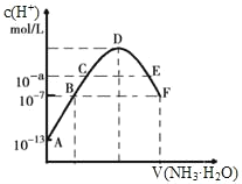
①NaHB溶液呈_______(填“酸性”“碱性”或“中性”)
②A、D、E三点溶液的pH由大到小为:_______
③F点溶液c(NH4+)_______2c(B2-)(填“>”“<”或“=”)
(2)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/LNaOH溶液,制得等量Mg(OH)2沉淀。
①分别向两支试管中加入不同试剂,请填写下表中的实验现象(用下列选项中字母代号填写)
试管编号 | 加入试剂 | 实验现象 |
Ⅰ | 2滴0.1mol/LFeCl3溶液 | _______ |
Ⅱ | 4mL2mol/LNH4Cl溶液 | _______ |
A 白色沉淀转化为红褐色沉淀 B 白色沉淀不发生改变
C 红褐色沉淀转化为白色沉淀 D 白色沉淀溶解,得无色溶液
②同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的沉淀溶解平衡正向移动。猜想2:_______。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁固体盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明正确的是_______(填“猜想1”或“猜想2”)。