题目内容
【题目】Cu(In1-xGaxSe2)(简称CIGS)可作多晶膜太阳能电池材料,具有非常好的发展前景。
回答下列问题:
(1)已知铟的原子序数为49,基态铟原子的电子排布式为[Kr]___;Ga、In、Se,第一电离能从大到小顺序为___。
(2)硅与碳位于同主族,碳的化合物中往往有碳碳双键、碳碳三键,但是硅的化合物中只存在硅硅单键,其主要原因是___。常温常压下,SiF4呈气态,而SiCl4呈液态,其主要原因是___。
(3)31Ga可以形成GaCl3·xNH3(x=3、4、5、6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为___。
(4)SeO32-的立体构型为___;SeO2中硒原子采取杂化类型是___。
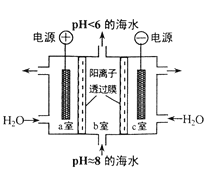
(5)常见的铜的硫化物有CuS和Cu2S两种。已知:晶胞中S2-的位置如图1所示,铜离子位于硫离子所构成的四面体中心,它们晶胞具有相同的侧视图如图2所示。已知CuS和Cu2S的晶胞参数分别为apm和bpm,阿伏加德罗常数的值为NA。
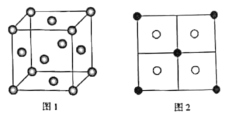
①CuS晶体中,相邻的两个铜离子间的距离为___pm。
②Cu2S晶体中,S2-的配位数为___。
③Cu2S晶体的密度为ρ=___g·cm-3(列出计算式即可)。
【答案】4d105s25p1 Se>Ga>In 硅原子半径大于碳,硅原子的原子轨道肩并肩重叠程度小,形成三键、三键不稳定 组成、结构相似、四氯化硅的相对分子质量较大 [Ga(NH3)4Cl2]Cl 三角锥形 sp2 ![]() a 8
a 8 ![]()
【解析】
Ga与In同主族,Se与Ga同周期;碳与硅同主族,碳原子半径小于硅原子半径;硒原子的价层电子数为4,其中为1个孤对电子对、3个成键电子对;CuS晶胞中S2-位于晶胞的顶点和面心上,铜离子位于体内,配位数为4。
(1)镓原子的质子数为49,电子排布是为1s22s22p63s23p63d104s24p64d105s25p1,简写为[Kr] 4d105s25p1;Ga与In同主族,Se与Ga同周期,同一主族从上到下第一电离能逐渐减小,同周期从左到右第一电离能逐渐增大,则第一电离能从大到小顺序为Se>Ga>In。
(2)碳碳双键、碳碳叁键都有![]() 键,硅原子的半径大于碳原子,硅原子的原子轨道肩并肩重叠程度小于碳原子,
键,硅原子的半径大于碳原子,硅原子的原子轨道肩并肩重叠程度小于碳原子,![]() 键不稳定。四氯化硅、四氟化硅都是分子构成的物质,组成、结构相似,四氯化硅的相对分子质量大于四氟化硅,故四氯化硅的分子间作用力较大,沸点较高。
键不稳定。四氯化硅、四氟化硅都是分子构成的物质,组成、结构相似,四氯化硅的相对分子质量大于四氟化硅,故四氯化硅的分子间作用力较大,沸点较高。
(3)向上述某配合物的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,两次沉淀的物质的量之比为1:2,说明该配合物内界和外界中含氯离子的个数比为2:1,由于Ga3+的配位数为6,则该配合物的化学式为[Ga(NH3)4Cl2]Cl。
(4)SeO32-中硒原子的价层电子对数为4,其中为1个孤对电子对、3个成键电子对,故它的立体构型为三角锥形;二氧化硒分子中硒原子价层有3个电子对,采取sp2杂化。
(5)①由题意可知,铜离子位于互不相邻的四面体中心,因此相邻的两个铜离子间的距离为![]() a pm。
a pm。
②铜离子配位数为4,根据化学式为Cu2S,得出S2-的配位数为8。
③Cu2S晶体中含有8个铜离子、4个硫离子,故晶体的密度为ρ=
![]() g·cm-3。
g·cm-3。