题目内容
27.2g某二价金属的氯化物ACl2中含有0.4mol Cl-离子,ACl2的摩尔质量是________g/mol,A的相对原子质量是________.
136 65
分析:先根据氯化物的分子式ACl2,由Cl-的物质的量求出氯化物的物质的量,再根据公式M=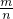 来确定分子的摩尔质量,摩尔质量在数值上和相对分子质量的大小相等,最后根据相对分子质量的大小确定金属元素的相对原子质量.
来确定分子的摩尔质量,摩尔质量在数值上和相对分子质量的大小相等,最后根据相对分子质量的大小确定金属元素的相对原子质量.
解答:因氯化物ACl2中含有0.4molCl-可知,氯化物ACl2的物质的量为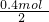 =0.2mol,则M(ACl2)=
=0.2mol,则M(ACl2)=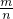 =
= =136g/mol,所以ACl2相对分子质量为136,
=136g/mol,所以ACl2相对分子质量为136,
则A的相对原子质量为136-35.5×2=65.故答案为:136g/mol;65.
点评:本题要求学生掌握化学式和化学式中离子的物质的量的关系,知道摩尔质量在数值上和相对分子质量的大小相等以及质量、摩尔质量、物质的量之间的关系.
分析:先根据氯化物的分子式ACl2,由Cl-的物质的量求出氯化物的物质的量,再根据公式M=
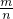 来确定分子的摩尔质量,摩尔质量在数值上和相对分子质量的大小相等,最后根据相对分子质量的大小确定金属元素的相对原子质量.
来确定分子的摩尔质量,摩尔质量在数值上和相对分子质量的大小相等,最后根据相对分子质量的大小确定金属元素的相对原子质量.解答:因氯化物ACl2中含有0.4molCl-可知,氯化物ACl2的物质的量为
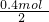 =0.2mol,则M(ACl2)=
=0.2mol,则M(ACl2)=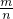 =
= =136g/mol,所以ACl2相对分子质量为136,
=136g/mol,所以ACl2相对分子质量为136,则A的相对原子质量为136-35.5×2=65.故答案为:136g/mol;65.
点评:本题要求学生掌握化学式和化学式中离子的物质的量的关系,知道摩尔质量在数值上和相对分子质量的大小相等以及质量、摩尔质量、物质的量之间的关系.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 ol Cl-离子,ACl2的摩尔质量是 ,A的相对原子质量是 。
ol Cl-离子,ACl2的摩尔质量是 ,A的相对原子质量是 。