题目内容
在4L密闭容器中充入6molA气体和5 molB气体,一定的条件下发生反应:3A(g)+B(g)![]() 2C(g)+xD(g)
2C(g)+xD(g)
500秒后达到平衡,生成2molC,而D浓度为0.5mol/L,下列判断正确的是( )
A.反应前20分钟,C的平均生成速率为4×10-3mol/L.s。
B.平衡时A、B的物质的量浓度相等
C.达到平衡后,压缩容器,平衡向正反应方向移动
D.平衡时,B物质的转化率为20%
D
【解析】 本题考查化学反应速率和化学平衡的相关计算。前20分钟内vC=2/(4×20×60)=4.2×10-4(mol/L·s),A错;平衡时,生成2mol C,同时消耗3 molA,1 mol B,所以平衡时剩余3 molA,4molB,其物质的量浓度不相等,B错;平衡时,D的浓度为0.5mol/L,可知其物质的量为2mol,与C相等,所以x=2,该反应前后体积不变,加压或减压,平衡均不移动,故C错;平衡时,B转化了1 mol,其转化率为1/5×100%=20%。选D。

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
 2C(g)+xD(g),10min达到化学平衡,生成了2mol C,经测定D的平均反应速率为0.05mol?L-1?min-1.下列判断正确的是( )
2C(g)+xD(g),10min达到化学平衡,生成了2mol C,经测定D的平均反应速率为0.05mol?L-1?min-1.下列判断正确的是( )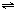 2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度为0.5mol?L-1,下列判断正确的是( )
2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度为0.5mol?L-1,下列判断正确的是( ) 2C(g)+xD(g),10min达到化学平衡,生成了2mol C,经测定D的平均反应速率为0.05mol?L-1?min-1.下列判断正确的是( )
2C(g)+xD(g),10min达到化学平衡,生成了2mol C,经测定D的平均反应速率为0.05mol?L-1?min-1.下列判断正确的是( )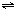 2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度为0.5mol?L-1,下列判断正确的是( )
2C(g)+xD(g),达到平衡时,生成了2molC,经测定D的浓度为0.5mol?L-1,下列判断正确的是( )