题目内容
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的操作是( )A.向水中投入一小块金属钠 B.将水加热煮沸
C.向水中通入二氧化碳气体 D.向水中加食盐晶体
解析:2Na+2H2O![]() 2NaOH+H2↑,由于NaOH的存在,破坏了水的电离平衡,但此时溶液中c(OH-)>c(H+),故A错误。将水加热煮沸,水的电离平衡向右移动,但c(H+)=c(OH-),故B错误。向水中通入二氧化碳,则CO2+H2O
2NaOH+H2↑,由于NaOH的存在,破坏了水的电离平衡,但此时溶液中c(OH-)>c(H+),故A错误。将水加热煮沸,水的电离平衡向右移动,但c(H+)=c(OH-),故B错误。向水中通入二氧化碳,则CO2+H2O![]() H2CO3
H2CO3![]() H++
H++![]() ,H+使水的电离平衡破坏,且c(H+)>c(OH-),故C正确。水中加食盐没有破坏水的电离平衡,故D错误。
,H+使水的电离平衡破坏,且c(H+)>c(OH-),故C正确。水中加食盐没有破坏水的电离平衡,故D错误。
答案:C

练习册系列答案
相关题目
能影响水的电离平衡,并使溶液中c(H+)>c(OH-)的措施是( )
| A、将水加热至100℃,测得pH=6 | B、向纯水中投入一小块金属钠 | C、向水中加入NH4Cl固体 | D、向水中加入Na2CO3固体 |
下列几种微粒中能影响水的电离平衡,且能使水的电离平衡向右移动的是( )
| A、HSO4- | B、Cl- | C、aX+ 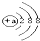 | D、bX2- 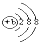 |
能影响水的电离平衡,并使溶液中的c(H+)>c(OH-)的措施是( )
| A、向水中通入SO2 | B、将水加热煮沸 | C、向纯水中投入一小块金属钠 | D、向水中加入NaCl |
下列各组离子中,每个离子都能影响水的电离平衡的一组是( )
| A、Ag+、HCO3-、PO43-、SO42- | B、Br -、Al3+、H+、CO32- | C、Fe2+、SO32-、CH3COO -、S2- | D、ClO-、OH-、Cu2+、Ba2+ |