题目内容
能量最低原理
原子核外电子的排布遵循 ,按轨道能量 依次排列,使整个原子处于能量 状态.
原子核外电子的排布遵循
考点:原子核外电子的能级分布,原子核外电子排布
专题:原子组成与结构专题
分析:在不违反泡利原理、和洪特规则的条件下,电子优先占据能量较低的原子轨道,使整个原子体系能量处于最低,据此分析解答.
解答:
解:泡利不相容原理:每个原子轨道上最多只能容纳 2个自旋状态 相反的电子;
洪特规则:在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同,
多电子原子核外电子排布遵循构造原理:即泡利不相容原理、洪特规则、能量最低原理,能量最低原理指:原子核外电子先占有能量较低的轨道.然后依次进入能量较高的轨道;使整个原子处于能量最低状态,
故答案为:构造原理;由低到高;最低.
洪特规则:在等价轨道(相同电子层、电子亚层上的各个轨道)上排布的电子将尽可能分占不同的轨道,且自旋方向相同,
多电子原子核外电子排布遵循构造原理:即泡利不相容原理、洪特规则、能量最低原理,能量最低原理指:原子核外电子先占有能量较低的轨道.然后依次进入能量较高的轨道;使整个原子处于能量最低状态,
故答案为:构造原理;由低到高;最低.
点评:本题考查了原子结构构造原理,明确能量最低原理是解本题关键,难度不大,注意基础知识的积累.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
Al2(SO4)3溶液的物质的量浓度为c mol/L.若已知该溶液含硫酸根离子n mol,则其体积应为( )
| A、1000n/3c mL |
| B、2n/3c mL |
| C、3c/1000n mL |
| D、n/3c mL |
有X、Y、Z、W、M五种短周期元素,其中X、Y、Z、W同周期,Z、M同主族;X+与M2-具有相同的电子层结构;离子半径:Z2->W-;Y的单质晶体熔点高、硬度大,是一种重要的半导体材料.下列说法中,正确的是( )
| A、X、M两种元素只能形成X2M型化合物 |
| B、Y是地壳中含量最多的元素,Y、W的单质可发生化合反应 |
| C、元素W和M的某些单质可作为水处理中的消毒剂 |
| D、由于W、Z、M元素的简单氢化物相对分子质量依次减小,所以其沸点依次降低 |
禁止工业酒精配制饮料,这是由于工业酒精中含有( )
| A、乙二醇 | B、丙三醇 |
| C、甲醇 | D、氯仿 |
有关有机物的下列说法中正确的是( )
| A、汽油、煤油和植物油都是烃的混合物 |
| B、甲烷、乙烯和苯在工业上都可以通过煤干馏得到 |
| C、分子式为C8H6O2的芳香族有机物分子中不可能有羧基 |
| D、含五个碳原子的有机物,分子中最多可形成四个碳碳单键 |
烯烃复分解反应是指在金属钨或钼等催化剂的作用下,碳碳双键断裂并重新组合的过程.例如:

则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的是( )
①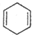 ②CH2=CH2③
②CH2=CH2③ ④CH2=C=CH2.
④CH2=C=CH2.

则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的是( )
①
 ②CH2=CH2③
②CH2=CH2③ ④CH2=C=CH2.
④CH2=C=CH2.| A、只有③ | B、只有②③ |
| C、只有①②③ | D、有①②③④ |
下列实验能证明一定有二氧化硫存在的是( )
①能使澄清石灰水变浑浊
②能使品红溶液褪色
③能使湿润的蓝色石蕊试纸变红
④通入足量的NaOH溶液,再加入BaCl2溶液有白色沉淀产生,该沉淀溶于盐酸
⑤通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
①能使澄清石灰水变浑浊
②能使品红溶液褪色
③能使湿润的蓝色石蕊试纸变红
④通入足量的NaOH溶液,再加入BaCl2溶液有白色沉淀产生,该沉淀溶于盐酸
⑤通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
| A、都不能 | B、都能 |
| C、②④⑤ | D、只有⑤ |
下列有关晶体的叙述,错误的是( )
| A、金刚石的网状结构中,由共价键形成的最小碳环上有6个碳原子 |
| B、在NaCl晶体中,每个Na+(或Cl-)周围都紧邻有6个Cl-(或Na+) |
| C、干冰晶体中,粒子之间通过共价键结合 |
| D、离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏 |
