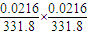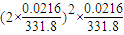题目内容
强电解质Ag2CrO4(M=331.8g?mol-1)的溶解度是0.0216g?L-1,则其浓度积Ksp为( )
分析:依据Ksp的计算表达式和溶解度概念分析计算得到,溶解度是0.0216g?L-1,可以利用为1L溶液中溶解的Ag2CrO4质量0.0216g,计算银离子和铬酸根离子浓度,结合溶度积常数计算式计算Ksp;
解答:解:溶解度是0.0216g?L-1,可以利用为1L溶液中溶解的Ag2CrO4质量0.0216g,n(Ag2CrO4)=
=
mol,c(Ag+)=2×
mol/L;c(CrO42-)=
mol/L;强电解质Ag2CrO4中存在沉淀溶解平衡,依据Ksp=c2(Ag+)c(CrO42-)=(2×
)2×
;
故选D.
| 0.0216g |
| 331.8g/mol |
| 0.0216 |
| 31.8 |
| 0.0216 |
| 31.8 |
| 0.0216 |
| 31.8 |
| 0.0216 |
| 31.8 |
| 0.0216 |
| 31.8 |
故选D.
点评:本题考查了沉淀溶解平衡的分析判断,溶度积常数计算应用,理解溶解度是解题关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
弱电解质和强电解质的本质区别在于( )
| A、离子数目的多少 | B、物质的量浓度相同时,溶液的导电能力 | C、在水溶液中是否存在电离平衡 | D、物质中所含化学键的不同 |