��Ŀ����
����Ŀ����Ԫ�صĵ��ʼ��仯�����ڹ�ũҵ������������������Ҫ���á�
(1)��֪����Ӧi��N2(g)+3H2(g)2NH3(g) ��H����92.4kJ/mol
��Ӧii��2H2(g)+O2(g)=2H2O(g) ��H����483.6kJ/mol
������ȫȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ_____��
(2)��֪��Ӧi�Ͽ�1mol��ѧ��������������±���
N��N | H��H | N��H | |
����/kJ��mol��1 | 945 | 436 | �� |
��Ͽ�1molN��H�������������_______kJ
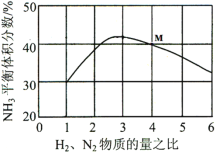
(3)��ͼ��ʾ��Ӧi��500�桢60.0MPa�����£�ԭ����Ͷ�ϱ���ƽ��ʱNH3��������Ĺ�ϵ������ͼ��M�����ݼ���N2��ƽ���������______���÷�Ӧ�Ļ�ѧƽ�ⳣ��K�ı���ʽ______��
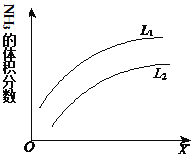
(4)��ͼ�Ǻϳɰ���Ӧƽ��������NH3������������¶Ȼ�ѹǿ�仯�����ߣ�ͼ��L(L1��L2)��X�ֱ�����¶Ȼ�ѹǿ������X��������______(�����¶�������ѹǿ��)���ж�L1��L2�Ĵ�С��ϵ��˵������_______��
(5)�绯ѧ���������������ڼ�����NH3�ĺ������乤��ԭ����ͼ��ʾ��
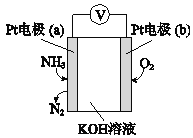
�ٷ�Ӧ����NH3��O2�����ʵ���֮��Ϊ____��
��a���ĵ缫��ӦʽΪ______��
���𰸡�4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ��H=��1266kJ/mol 390.9 8%  ѹǿ L1��L2�ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ��ѹǿ��ͬʱ���¶����ߣ�ƽ�������ƶ����������������С 4:3 2NH3�C6e��+6OH��=N2+6H2O
ѹǿ L1��L2�ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ��ѹǿ��ͬʱ���¶����ߣ�ƽ�������ƶ����������������С 4:3 2NH3�C6e��+6OH��=N2+6H2O
��������
���ݸ�˹���ɣ���Ӧ�ȼ���ʽ�ش����⣬��ͬ�����£���������ȵ����������ʵ���֮�ȣ�ͨ������ʽ����ƽ���������������ԭ���ԭ���ж�����������������������Ӧ��
(1)���ݸ�˹���ɣ�������ȫȼ�����ɵ�����ˮ�������Ȼ�ѧ����ʽ4NH3(g)+3O2(g)=2N2(g)+6H2O(g)��H=92.4��2kJ/mol��483.6��3kJ/mol=��1266kJ/mol��
(2)������H=��Ӧ�����-��������ܿ�֪���Ͽ�1molN��H�������������![]() kJ��
kJ��
(3)����ͼ��M�����ݣ���ʱ������������Ͷ�ϱ�Ϊ1��4��������ƽ���������Ϊ40%���跴Ӧǰ����������1mol������������4mol��ƽ��ʱ��Ӧ�����˵���xmol�����ݷ�ӦN2+3H22NH3������ʽ��

ƽ��ʱ�������������Ϊ![]() ��x=
��x=![]() ����N2��ƽ���������
����N2��ƽ���������![]() ���÷�Ӧ�Ļ�ѧƽ�ⳣ��K�ı���ʽΪ
���÷�Ӧ�Ļ�ѧƽ�ⳣ��K�ı���ʽΪ ��
��
(4)�ϳɰ���ӦΪ���ȷ�Ӧ����Ӧ���������������С���ʱ���L���䣬�۲�����һ�����ߣ�����X�������������������˵����Ӧ�����ƶ���������������ԭ����XΪѹǿ��LΪ�¶ȣ�L1��L2���ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ��ѹǿ��ͬʱ���¶����ߣ�ƽ�������ƶ����������������С��
(5)����ͼ������Ӧ���ɵ����������ϼ����ߣ�����������Ӧ��Ϊ��������������b�缫������ԭ��Ӧ��Ϊ������
�ٷ�Ӧ�ܷ���Ϊ4NH3+3O2=2N2+6H2O����Ӧ����NH3��O2�����ʵ���֮��Ϊ4��3��
��a��Ϊ����������������Ӧ���缫��ӦʽΪ2NH3�C6e��+6OH��=N2+6H2O��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�����Ŀ����֪t��ʱ��ijЩ���ʵ�ƽ�ⳣ��K��ֵ�����ʾ������˵���������(����)
���� | HCIO | H2CO3 | AgCl | AgI |
ƽ�ⳣ�� | Ka��10��9 | K��10��7 K��10��11 | Ksp��1.8��10��10 | Ksp��8.51��10��17 |
A.��������ˮ�м�������NaHCO3��ǿ��ˮƯ����
B.��ͬ�¶Ⱥ�Ũ���£�NaClO��Һ��pH��Na2CO3��Һ��pHС
C.t��ʱ��AgCl(s)+I��(aq)![]() AgI(s)+Cl��(aq)��ƽ�ⳣ��K��2.1��106
AgI(s)+Cl��(aq)��ƽ�ⳣ��K��2.1��106
D.��AgCl��AgI�ı�����Һ�������ϣ��ټ�������AgNO3��Һ�������ɵ�����AgCl��AgI����
����Ŀ���˰�ȫ���������Ⱦ����������㷺��ע���ڱ�ը�ĺ˵�վ��Χ���з��������� ��-131��-137����-131 �������������룬���ܻ�������״���״�ȼ�����
(1)����ͬ�����ǰ������(������������)������Ԫ��X��Y��Z�ĵ�һ���������±���
Ԫ�ش��� | X | Y | Z |
��һ������/(kJ.mol) | 520 | 496 | 419 |
��̬Zԭ�ӵ����ڶ�����ӵ��Ų�ʽΪ______��X��Y��Z����Ԫ���γɵĵ����۵��ɸߵ��͵�˳��Ϊ_______(��Ԫ�ط��ű�ʾ)����ԭ��Ϊ___________ .
(2)F��Iͬ����,BeF2��������ԭ�ӵ��ӻ�����Ϊ_________ ,BeF2������________����(ѡ���������������Ǽ�����)��
(3)��֪�ߵ�����������ʽ,��ѧʽ�ֱ�ΪH5IO6  ��HIO4 ,��������ǿ��˳��Ϊ:H5IO6 ________HIO4(ѡ��">"��"<"��=��)���ӵ����Ƶ��ص���ʽ�ĽǶȷ���,H5IO6�����еĻ�ѧ����________(д������).
��HIO4 ,��������ǿ��˳��Ϊ:H5IO6 ________HIO4(ѡ��">"��"<"��=��)���ӵ����Ƶ��ص���ʽ�ĽǶȷ���,H5IO6�����еĻ�ѧ����________(д������).
(4)131I2����ľ����ṹ��ͼ����ʾ���þ�����ƽ������________��131Iԭ�ӣ������е���ӵ�������_________�ֲ�ͬ�ķ���

(5)KI�ľ����ṹ��ͼ����ʾ��ÿ��K����Χ���ڵ�K������Ϊ_______����KI������ܶ�Ϊ��g.cm-3 ,K��I��ԭ�Ӱ뾶�ֱ�Ϊrkcm��rI cm,�����ӵ�������ֵΪNA,�� KI�����еĿռ�������Ϊ_______. �ۿռ�������=(�����/�������)��100%,�������ĸ�Ĵ���ʽ��ʾ���ɣ�



