题目内容
 如图,A、B、C、D、E各代表铁、水、三氧化硫、盐酸和氢氧化钡中的一种物质.在常温下,相连环物质之间能发生反应,不相连环物质之间不能发生反应.且B的相对分子质量小于D.
如图,A、B、C、D、E各代表铁、水、三氧化硫、盐酸和氢氧化钡中的一种物质.在常温下,相连环物质之间能发生反应,不相连环物质之间不能发生反应.且B的相对分子质量小于D.(1)五种物质中属于氧化物的有
H2O、SO3
H2O、SO3
(填化学式);(2)请写出氢氧化钡的电离方程式
Ba(OH)2=Ba2++2OH-
Ba(OH)2=Ba2++2OH-
;(3)请写出铁与水蒸气在高温下发生反应的化学方程式
3Fe+4H2O(g)
Fe3O4+4H2
| ||
3Fe+4H2O(g)
Fe3O4+4H2
;
| ||
(4)请写出下列物质的化学式:B
HCl
HCl
,DSO3
SO3
.分析:题中常温下铁只能和盐酸反应,水只能与三氧化硫反应,而盐酸能和铁、氢氧化钡反应,三氧化硫与水、氢氧化钡反应,则B、D肯定为盐酸和三氧化硫中的物质,因B的相对分子质量小于D,则B为HCl,D为SO3,所以A为铁,C为水氢氧化钡,E为水,结合对应物质的性质解答该题.
解答:解:题中常温下铁只能和盐酸反应,水只能与三氧化硫反应,而盐酸能和铁、氢氧化钡反应,三氧化硫与水、氢氧化钡反应,则B、D肯定为盐酸和三氧化硫中的物质,因B的相对分子质量小于D,则B为HCl,D为SO3,所以A为铁,C为水氢氧化钡,E为水,
(1)五种物质中属于氧化物的有H2O、SO3,故答案为:H2O、SO3;
(2)氢氧化钡为强电解质,电离出钡离子和氢氧根离子,电离方程式为Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-;
(3)铁与水蒸气在高温下发生反应生成四氧化三铁和氢气,反应的方程式为3Fe+4H2O(g)
Fe3O4+4H2,
故答案为:3Fe+4H2O(g)
Fe3O4+4H2;
(4)由以上分析可知B为HCl,D为SO3,故答案为:HCl;SO3.
(1)五种物质中属于氧化物的有H2O、SO3,故答案为:H2O、SO3;
(2)氢氧化钡为强电解质,电离出钡离子和氢氧根离子,电离方程式为Ba(OH)2=Ba2++2OH-,故答案为:Ba(OH)2=Ba2++2OH-;
(3)铁与水蒸气在高温下发生反应生成四氧化三铁和氢气,反应的方程式为3Fe+4H2O(g)
| ||
故答案为:3Fe+4H2O(g)
| ||
(4)由以上分析可知B为HCl,D为SO3,故答案为:HCl;SO3.
点评:本题考查无机物的推断,侧重于学生的分析能力和元素化合物知识的综合运用,注意把握物质的性质,题中B的相对分子质量小于D是解答该题的突破口,答题时注意体会.

练习册系列答案
相关题目
 下列有关实验的操作、现象和原理,正确的是( )
下列有关实验的操作、现象和原理,正确的是( )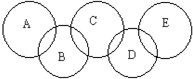 如图,A、B、C、D、E各代表碳、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质.一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空:
如图,A、B、C、D、E各代表碳、铁、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质.一定条件下,相连环物质间能发生反应,不相连环物质间不能发生反应,且B的相对分子质量大于D.请填空: 如图中A、B、C、D是同周期或同主族的相邻元素:
如图中A、B、C、D是同周期或同主族的相邻元素: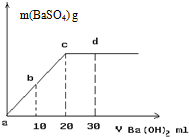 (1)服用含碘化钾的碘药片可抗核辐射.将碘片剥去糖衣皮研粹后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色,试回答下列问题:
(1)服用含碘化钾的碘药片可抗核辐射.将碘片剥去糖衣皮研粹后置于试管中制得无色水溶液,并加入几滴淀粉试液,然后向试管中逐滴加入氯水,观察到溶液由无色变为蓝色,若继续滴加氯水后蓝色溶液又褪为无色,试回答下列问题: