题目内容
25 ℃时,水的电离达到平衡:H2O H++OH-;△H>0,下列叙述正确的是
H++OH-;△H>0,下列叙述正确的是
A.向水中加入少量固体NaHSO4,c(H+)增大,KW不变
B.向水中加入少量NaOH溶液,平衡逆向移动,c(OH-)降低
C.向水中加入少量CH3COONa固体,平衡逆向移动,c(H+)降低
D.将水加热,KW增大,pH不变
【答案】
A
【解析】
试题分析:A选项,加入NaHSO4,硫酸氢根电离出氢离子,故c(H+)增大。KW只与温度有关,故不变。B选项,加入氢氧化钠溶液,溶液PH增大,故c(OH-)增大。错误。C选项,向水中加入少量CH3COONa固体,醋酸根与水电离出的氢离子形成醋酸弱电解质,平衡向正反应方向移动,c(H+)降低 。故错误。D选项,加入热水,温度升高,KW值增大,PH值增大。错误。
考点:弱电解质电离平衡

练习册系列答案
相关题目
25℃时,水的电离达到平衡:H2O?H++OH-,下列叙述正确的是( )
| A、将纯水加热到95℃时,Kw变大,pH不变,水仍呈中性 | B、向纯水中加入稀氨水,平衡逆向移动,c(OH-)增大,Kw变小 | C、向纯水中加入少量固体碳酸钠,c(H+)减小,Kw不变,影响水的电离平衡 | D、向纯水中加入醋酸钠或盐酸,均可抑制水的电离,Kw不变 |
 水的电离平衡曲线如图所示.?
水的电离平衡曲线如图所示.? 已知水在25℃和95℃时,其电离平衡曲线如图所示:
已知水在25℃和95℃时,其电离平衡曲线如图所示: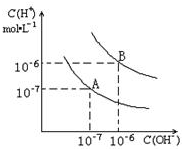
 H++OH-;△H>0,下列叙述正确的是
H++OH-;△H>0,下列叙述正确的是