题目内容
有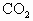 、
、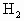 、HCl的混合气体100mL.将此混合气通过足量的
、HCl的混合气体100mL.将此混合气通过足量的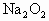 固体,充分反应后,气体体积变为60mL,再将所得气体点火爆炸完全反应后,降至室温恰好无气体剩余.试求混合气中各成分的体积.(气体体积均在同温、同压下测得,假设HCl可与
固体,充分反应后,气体体积变为60mL,再将所得气体点火爆炸完全反应后,降至室温恰好无气体剩余.试求混合气中各成分的体积.(气体体积均在同温、同压下测得,假设HCl可与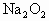 完全反应)
完全反应)
答案:
解析:
解析:
|
解: 根据题意,反应完成后无气体,则 根据:
解后得:x=20mL( y=40mL(HCl) 答:略. |

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
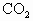 和HCl均可与
和HCl均可与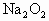 反应,设原混合气中含
反应,设原混合气中含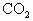 体积为x,HCl体积为y,则
体积为x,HCl体积为y,则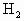 为(100-x-y)mL.
为(100-x-y)mL.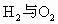 恰好反应.
恰好反应.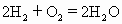 ,所以60mL的气体中应为40mL的
,所以60mL的气体中应为40mL的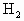 和20mL的
和20mL的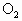 .
.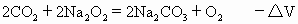

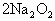 +4HCl=4NaCl+
+4HCl=4NaCl+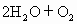 -△V
-△V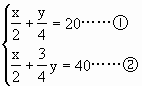
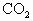 )
)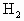 为40mL
为40mL (2009?清远模拟)某校学生在实验室中设计了如下装置,模拟侯德榜制碱法,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,再将碳酸氢钠晶体加热分解而制得碳酸钠晶体,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和:
(2009?清远模拟)某校学生在实验室中设计了如下装置,模拟侯德榜制碱法,获得碳酸氢钠晶体,反应原理可用如下化学方程式表示:NH3+CO2+NaCl+H2O═NH4Cl+NaHCO3↓,依据此原理,再将碳酸氢钠晶体加热分解而制得碳酸钠晶体,其中B装置中的试管内是溶有氨和氯化钠的溶液,且二者均已达到饱和: