题目内容
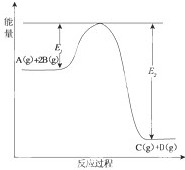 某可逆反应的反应过程中能量变化如图所示,回答下列问题.
某可逆反应的反应过程中能量变化如图所示,回答下列问题.(1)若E1=215kJ?mol-1,E2=625kJ?mol-1,则该反应的热化学方程式为:A(g)+2B(g)═C(g)+D(g)△H=
-410kJ?mol-1
-410kJ?mol-1
.(2)当反应达到平衡时,降低温度,A的转化率增大
增大
增大
(填“增大”“减小”或“不变”),原因是_降低温度,平衡朝放热方向移动,即朝正方向移动降低温度,平衡向放热反应方向(即正反应方向)移动,A的转化率增大
降低温度,平衡向放热反应方向(即正反应方向)移动,A的转化率增大
.(3)在反应体系中加入催化剂,反应速率增大,则
A
A
(用字母代号填空).
A.E1减小,E2减小,反应热不变
B.E1减小,E2减小,反应热减小
C.E1减小,E2增大,反应热减小
D.E1增大,E2增大,反应热增大.
分析:(1)依据图象分析焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量,结合然后方程式书写方法标注物质聚集状态和对应焓变;
(2)反应是放热反应降温平衡正向进行;
(3)催化剂同等程度改变正逆反应速率,降低反应所需的活化能,不影响平衡移动.
(2)反应是放热反应降温平衡正向进行;
(3)催化剂同等程度改变正逆反应速率,降低反应所需的活化能,不影响平衡移动.
解答:解:(1)焓变=反应物断裂化学键吸收的能量-生成物形成化学键放出的能量=215KJ/mol-625KJ/mol=-410KJ/mol,反应的热化学方程式为:A(g)+2B(g)=C(g)+D(g)△H=-410kJ?mol-1,故答案为:-410kJ?mol-1;
(2)当反应达到平衡时,反应是放热反应,降低温度,平衡正向进行,A的转化率增大;
故答案为:增大;降低温度,平衡向放热反应方向(即正反应方向)移动,A的转化率增大;
(3)在反应体系中加入催化剂,催化剂改变反应速率,不改变化学平衡,反应热不变,催化剂同等程度改变正反应速率和逆反应速率,降低反应所需的活化能,则E1减小,E2减小,故答案为:A.
(2)当反应达到平衡时,反应是放热反应,降低温度,平衡正向进行,A的转化率增大;
故答案为:增大;降低温度,平衡向放热反应方向(即正反应方向)移动,A的转化率增大;
(3)在反应体系中加入催化剂,催化剂改变反应速率,不改变化学平衡,反应热不变,催化剂同等程度改变正反应速率和逆反应速率,降低反应所需的活化能,则E1减小,E2减小,故答案为:A.
点评:本题考查化学反应能量变化计算方法,化学平衡的影响因素和平衡移动方向的判断,平衡常数随温度变化是注意问题,题目难度中等.

练习册系列答案
相关题目
下列关于反应过程中能量变化的说法正确的是( )


| A、在一定条件下,某可逆反应的△H=+100kJ?mol-1,则该反应正反应活化能比逆反应活化能大100kJ?mol-1 | B、图中A、B曲线可分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)△H>0未使用和使用催化剂时,反应过程中的能量变化 | C、同温同压下,反应H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同 | D、己知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2.则△H1>△H2 |
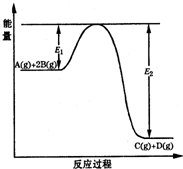 某可逆反应的反应过程中能量变化如图所示,回答下列问题.
某可逆反应的反应过程中能量变化如图所示,回答下列问题.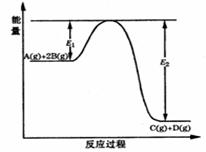 (2)当反应达到平衡时,降低温度,A的转化率
(2)当反应达到平衡时,降低温度,A的转化率