��Ŀ����
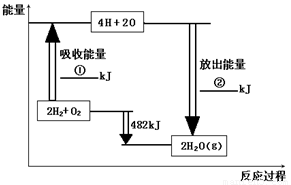
(8��)��֪��1mol�����еĻ�ѧ����Ҫ����436kJ��������1mol�����еĻ�ѧ����Ҫ����498kJ����������ͼ�е�����ͼ���ش��������⣺
��1���ֱ�д���٢ڵ���ֵ��
�� �� �� �� �� ��
��2������H2O��g���е�1mol H-O���ų� �� kJ��������
��3����֪��H2O��l��= H2O��g�� DH = +44 kJ��mol��1 ����д����������������ȫȼ������Һ̬ˮ���Ȼ�ѧ����ʽ�� �� ��
(8��)
��1�� �� 1370 (2��) �� 1852 (2��) ��2��463 (2��)
��3��2H2��g��+ O2��g��= 2H2O��l�� ��H = ��570kJ��mol��1 (2��)
��״̬����ƽ�����š���ֵ�͵�λ��ֻҪ��һ���Ͳ�����)
����:

��ϰ��ϵ�д�
�����Ŀ
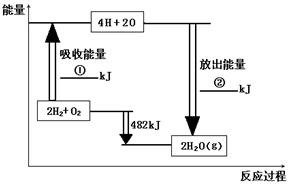
 O2(g) �� H2O(g) ��H����241.8 kJ��mol��1
O2(g) �� H2O(g) ��H����241.8 kJ��mol��1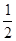 O2(g) �� H2O(g)
��H����241.8 kJ��mol��1
O2(g) �� H2O(g)
��H����241.8 kJ��mol��1