题目内容
1.现有赤铁矿(主要成分是Fe2O3,假设其他成分不含铁元素)16g,用氢气还原,得到单质6.72g,则该赤铁石中Fe2O3的质量分数为( )| A. | 42% | B. | 60% | C. | 70% | D. | 80% |
分析 用氢气还原,得到单质6.72g为Fe的质量,m(Fe2O3)=m(赤铁矿)×w(Fe2O3),而m(Fe)=m(Fe2O3)×$\frac{112}{160}$.
解答 解:用氢气还原,得到单质6.72g为Fe的质量,则:16g×w(Fe2O3)×$\frac{112}{160}$=6.72g,解得w(Fe2O3)=60%,
故选:B.
点评 本题考查化学式计算、质量分数计算,比较基础,注意对基础知识的理解掌握.

练习册系列答案
 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
11.设NA为阿伏加德罗常数,下列说法正确的是( )
| A. | 2.4g金属镁变成镁离子时失去的电子数为0.2NA | |
| B. | 常温常压下,1mol氦气所含原子数为2NA | |
| C. | 标准状况下,22.4L CCl4含有的氯原子数为4NA | |
| D. | 0.5mol•L-1 Na2CO3溶液中含有Na+离子的数目为NA |
9.下列微粒中半径最小的是( )
| A. | Ca2+ | B. | K | C. | S2- | D. | K+ |
16.卤素构成一个性质相似,且有一定递变规律的元素族的基本依据是( )
| A. | 卤素都是活泼的金属元素 | |
| B. | 卤素是常见的成盐元素,都是氧化剂 | |
| C. | 卤素原子最外层都有7个电子 | |
| D. | 卤化氢、卤化银的性质都有相似之处 |
6.下列各组物质中,X是主体物质,Y是少量杂质,Z是除去杂质所要加入的试剂,其中所加试剂正确的一组是( )
| A | B | C | D | |
| X | FeCl2溶液 | FeCl3溶液 | Fe | Na2SO4溶液 |
| Y | FeCl3 | CuCl2 | Al | Na2CO3 |
| Z | Cl2 | Fe | NaOH溶液 | BaCl2溶液 |
| A. | A | B. | B | C. | C | D. | D |
13.常温下将盛有15mLNO2和20mLNO的混合气体的试管倒立于水槽中,并向其中通入O2一段时间后,试管内还剩余5mL气体,则通入O2的体积为( )
| A. | 8mL | B. | 10mL | C. | 15mL | D. | 23.75mL |
17.氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应属于区域3的是( ) 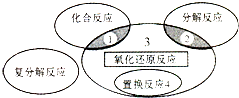

| A. | 4Fe(0H)2+O2+2H2O═4Fe(OH)3 | B. | 2H2O2$\frac{\underline{\;催化剂\;}}{\;}$2H2O+O2↑ | ||
| C. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$3CO2+2Fe | D. | Zn+H2SO4═ZnSO4+H2↑ |
18.下列事故处理不正确的是( )
| A. | 不慎把浓硫酸沾在手上,立即用干布拭去,再用水冲洗 | |
| B. | 不慎把苯酚沾在手上,立即用70℃以上的热水冲洗 | |
| C. | 金属钠着火,用泡沫灭火器扑灭 | |
| D. | 酒精灯不慎碰翻着火,用湿布盖灭 |